题目内容
8.对于某些离子的检验及结论正确的是( )| A. | 加盐酸有无色气体产生,该气体能使澄清石灰水变混浊,原溶液中一定有CO32- | |
| B. | 加氯化钡溶液有白色沉淀产生,再加盐酸,淀淀不消失,原溶液中一定有SO42- | |
| C. | 某溶液中加入Na2CO3溶液后有白色沉淀,则该溶液中一定有Ca2+ | |
| D. | 某溶液的焰色反应为黄色,则该溶液中一定有Na+ |
分析 A、盐酸能与含碳酸根或碳酸氢根离子的物质反应生成二氧化碳,二氧化碳气体遇澄清石灰水变浑浊;
B、氯化钡能与硫酸根离子或银离子结合生成不溶于水也不溶于酸的沉淀;
C、能和Na2CO3溶液反应生成白色沉淀的可能为Ca2+,也可能为Ba2+;
D、焰色反应为元素的性质.
解答 解:A、盐酸能与含碳酸根或碳酸氢根离子的物质反应生成二氧化碳,加入稀盐酸产生无色气体,不一定有CO32-,故A错误;
B、氯化钡能与硫酸根离子或银离子结合生成不溶于水也不溶于酸的沉淀,加入氯化钡溶液有白色沉淀产生,再加盐酸,沉淀不消失,不一定有SO42-,可能含有银离子,故B错误;
C、能和Na2CO3溶液反应生成白色沉淀的可能为Ca2+,也可能为Ba2+,故该溶液中不一定有Ca2+,故C错误;
D、焰色反应为元素的性质,某溶液的焰色反应为黄色,则该溶液中一定有Na+,故D正确;
故选D.
点评 本题考查了常见离子的检验,完成此题,可以依据已有的知识进行解答.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
19.已知NaH和H2O反应生成H2和NaOH,反应中1mol NaH( )
| A. | 得到1 mol e- | B. | 失去1 mol e- | C. | 失去2 mol e- | D. | 没有电子得失 |
3.将一定量的NaCl溶于90g水中,使每10个水分子中含有一个Cl-,则该NaCl的物质的量是( )
| A. | 0.05mol | B. | 0.1mol | C. | 0.25mol | D. | 0.5mol |
13.下列除去杂质的方法中正确的是( )
| A. | 苯甲醛中混有苯甲酸,加入生石灰,再加热蒸馏 | |
| B. | 乙醇中混有乙酸,加入NaOH溶液后,用分液漏斗分液 | |
| C. | 乙烷中混有乙烯,加入氢气在一定条件下充分反应 | |
| D. | 溴苯中混有溴,加入NaOH溶液后,用分液漏斗分液 |
20.用NA表示阿伏德罗常数,下列叙述正确的是( )
| A. | 标准状况下,22.4LH2O含有的分子数为1NA | |
| B. | 5.6g铁与足量氯气反应,转移的电子数目为0.3NA | |
| C. | 常温常压下,NA个CO2和CO分子占有的体积约为22.4L | |
| D. | 物质的量浓度为0.5mol/L的MgCl2溶液中,含有Cl-个数为1NA |
17.用如图表示的一些物质或概念间的从属关系中不正确的是( )
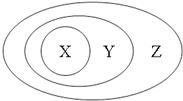

| A. | 铜ds区元素过渡元素 | B. | 明矾盐化合物 | ||
| C. | 胶体分散系混合物 | D. | 氧化钠金属氧化物碱性氧化物 |
13.美国的科学家发现普通盐水在无线电波的照射下可以燃烧,有望解决人类的能源危机.无线电频率可以降低盐水中所含元素之间的结合力,释放出氢气,一旦点火,氢气就会在这种频率下持续燃烧.上述“盐水中所含元素之间的结合力”是指( )
| A. | Na+与Cl-之间的离子键 | B. | 水分子间的氢键 | ||
| C. | 水分子内的共价键 | D. | 上述所有作用力 |
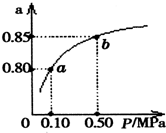 已知2A(g)+B(g)?2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.010mol•L-1,放出热量Q1kJ.
已知2A(g)+B(g)?2C(g),向容积为1L的密闭容器中加入0.050mol A和0.025mol B,在500℃时充分反应,达平衡后测得c(C)=0.010mol•L-1,放出热量Q1kJ.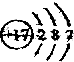 表示Cl(填写元素符号);
表示Cl(填写元素符号); ”表示一个氮原子,则“
”表示一个氮原子,则“ ”表示N2(填写粒子符号)
”表示N2(填写粒子符号)