题目内容
【题目】已知氨可以与热的氧化铜反应得到N2和金属铜,用如图中的装置可以实现该反应(夹持装置略去)。回答下列问题:
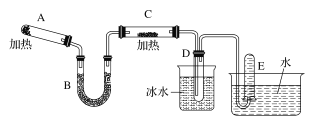
(1)A中发生反应的化学方程式是_____________。
(2)B中加入的物质是________。
(3)实验时在C中观察到的现象是________,发生反应的化学方程式是_______。
(4)检验D中收集到的物质的方法和现象是________________________。
【答案】2NH4Cl+Ca(OH)2![]() CaCl2+2NH3↑+2H2O 碱石灰(或CaO) 黑色粉末逐渐变为红色且右管口有水珠出现 2NH3+3CuO
CaCl2+2NH3↑+2H2O 碱石灰(或CaO) 黑色粉末逐渐变为红色且右管口有水珠出现 2NH3+3CuO![]() N2+3Cu+3H2O 用湿润的红色石蕊试纸,若变蓝则说明有NH3存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有NH3存在)。
N2+3Cu+3H2O 用湿润的红色石蕊试纸,若变蓝则说明有NH3存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有NH3存在)。
【解析】
(1)在实验室是用氯化铵与氢氧化钙反应生成氯化钙、氨气和水,化学方程式:Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O,故答案为:Ca(OH)2+2NH4Cl
CaCl2+2NH3↑+2H2O,故答案为:Ca(OH)2+2NH4Cl![]() CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(2)A装置制取的氨气中含有水蒸气,B中物质为碱性干燥剂如碱石灰或氧化钙,目的是用来干燥氨气,故答案为:碱石灰(或CaO)。
(3)经干燥后的氨气与CuO在加热时在装置C中反应反应:2NH3+3CuO![]() N2+3H2O+3Cu;反应产生了Cu,固体的物质有黑色变为红色;所以实验时C中观察到的现象是固体由黑色变为红色,故答案为:黑色粉末逐渐变为红色且右管口有水珠出现,2NH3+3CuO
N2+3H2O+3Cu;反应产生了Cu,固体的物质有黑色变为红色;所以实验时C中观察到的现象是固体由黑色变为红色,故答案为:黑色粉末逐渐变为红色且右管口有水珠出现,2NH3+3CuO![]() N2+3H2O+3Cu。
N2+3H2O+3Cu。
(4)氨气还原氧化铜之后剩余的是氨气和产生的水蒸气在冷凝时会形成氨水,具有氨气的成分,氨气可以使湿润的红色石蕊试纸变蓝或者用蘸有浓盐酸的玻璃棒放在容器口有白烟产生,故答案为:用湿润的红色石蕊试纸,若变蓝则说明有NH3存在(或用蘸有浓盐酸的玻璃棒放在容器口,若有白烟出现,也说明有NH3存在)。

【题目】实验室里有4个药品橱,已经存放以下列试剂:
药品橱 | 甲橱 | 乙橱 | 丙橱 | 丁橱 |
药品 | 醋酸,乙醇 | CuSO45H2O,MgCl2 | 白磷,硫黄 | 镁条,锌粒 |
实验室新购进一些碘化钾,应该将这些碘化钾放在( )
A.甲橱
B.乙橱
C.丙橱
D.丁橱