题目内容
如图所示的装置,X、Y都是惰性电极。将电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色。试回答下列问题: 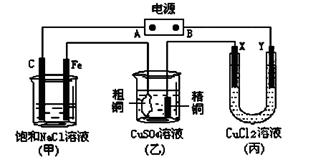
(1)在电源中,B电极为 极(填电极名称,下同);丙装置中Y电极为 极。
(2)在甲装置中,石墨(C)电极上发生 反应(填“氧化”或“还原”);甲装置中总的化学方程式是: 。
(3)丙装置在通电一段时间后,X电极上发生的电极反应式是 。
(4)如果乙装置中精铜电极的质量增加了0.64g,请问甲装置中,铁电极上产生的气体在标准状况下为
L。
(1)负极;阴极。 (2)氧化;2NaCl+2H2O 2NaOH+H2↑+Cl2↑
2NaOH+H2↑+Cl2↑
(3)2Cl--2e-=Cl2↑ (4)0.224L
解析试题分析:(1)由于电源接通后,向(甲)中滴入酚酞溶液,在Fe极附近显红色,说明在Fe电极附近的水溶液显碱性。则在该电极上是H+放电,所以根据同种电荷相互排斥,异种电荷相互吸引的原则Fe为阴极,与直流电源的负极相连。因此在电源中,B电极为负极,A电极为正极。在丙装置中Y电极为阴极。(2)在甲装置中,石墨(C)电极为电解池的阳极,在阳极上发生氧化反应。由于在NaCl溶液中放电能力Cl->OH-,所以在C上发生氧化反应2Cl—-2e-=Cl2↑. 甲装置中总的化学方程式是:2NaCl+2H2O Cl2↑+H2↑+2NaOH. (3)丙装置在通电一段时间后,阳极X电极上发生的电极反应式是2Cl--2e-=Cl2↑;(4)如果乙装置中精铜电极的质量增加了0.64g,n(Cu)=0.01mol。则n(e-)=0.02mol。由于在整个闭合回路中电子转移数目相等,所以铁电极上产生的氢气气体为0.01mol,在标准状况下为0.224L
Cl2↑+H2↑+2NaOH. (3)丙装置在通电一段时间后,阳极X电极上发生的电极反应式是2Cl--2e-=Cl2↑;(4)如果乙装置中精铜电极的质量增加了0.64g,n(Cu)=0.01mol。则n(e-)=0.02mol。由于在整个闭合回路中电子转移数目相等,所以铁电极上产生的氢气气体为0.01mol,在标准状况下为0.224L
考点:考查电源电极的确定及电解反应原理的应用的知识。

某化学兴趣小组为了探索铝电极在原电池中的作用,设计并进行了以下一系列实验,实验结果记录如下:
| 编号 | 电极材料 | 电解质溶液 | 电流计指针偏转方向 |
| ① | Mg 、Al | 稀盐酸 | 偏向Al |
| ② | Al、Cu | 稀盐酸 | 偏向Cu |
| ③ | Al、石墨 | 稀盐酸 | 偏向石墨 |
| ④ | Mg、Al | NaOH溶液 | 偏向Mg |
| ⑤ | Al、Zn | 浓硝酸 | 偏向Al |
根据上表中的实验现象完成下列问题:
(1)实验①、②中Al所作的电极是否相同?
答:____________________________________________
(2)写出实验③中的电极名称、电极反应式和电池总反应方程式。铝为( )______________________________
石墨为( )__________________________
电池总反应:__________________________
(3)实验④中的铝作________极。
(4)实验⑤中铝作________极。





