题目内容
1.二氯化二硫(S2Cl2)是广泛用于橡胶工业的硫化剂,其分子结构如图所示.常温下,S2Cl2是一种橙黄色液体,遇水易水解,产生能使品红褪色的气体,且溶液变浑浊.下列说法正确的是( )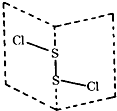
| A. | S2Cl2的分子中各原子最外层都为8电子结构 | |
| B. | S2Cl2是氧化剂,水是还原剂 | |
| C. | 将反应后所得的溶液滴入碳酸氢钠溶液中有气泡产生 | |
| D. | 反应中,生成1mol气体,转移电子为2mol |
分析 A、由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,写出电子式确定每个原子周围的电子数;
B、S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S);
C、根据亚硫酸酸性比碳酸强判断;
D、S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分从+1升高到+4价(生成SO2),据此计算.
解答 解:A.由结构可知,S2Cl2分子中S原子之间形成1对共用电子对,Cl原子与S原子之间形成1对共用电子对,S2Cl2的电子式为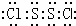 ,每个原子周围都满足8电子稳定结构,故A正确;
,每个原子周围都满足8电子稳定结构,故A正确;
B.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分升高到+4价(生成SO2),一部分降低到0价(生成S),所以S2Cl2既是氧化剂又是还原剂,故B错误;
C.因为亚硫酸酸性比碳酸强,所以将反应后所得的溶液即亚硫酸滴入碳酸氢钠溶液中发生反应生成二氧化碳气体,故C正确;
D.S2Cl2遇水易水解,并产生能使品红溶液褪色的气体,该气体为二氧化硫,在反应过程中硫元素一部分从+1升高到+4价(生成SO2),所以生成1mol气体,转移电子为3mol,故D错误.
故选AC.
点评 本题以S2Cl2的结构为载体,考查分子结构、氧化还原反应等,难度不大,是对基础知识的综合运用与学生能力的考查,注意基础知识的全面掌握.

练习册系列答案
相关题目
12.下列用连线方法对部分化学知识进行归纳的内容中,有错误的组是( )
| A. | 物质的性质与用途: 磺胺类药物能抑制细菌合成核酸--治疗肺炎、脑膜炎、尿路感染、呼吸道感染 酸能与碱中和-----胃酸过多的病人服用含氢氧化镁的药物 | |
| B. | 保护环境: 控制“白色污染”--禁止使用所有塑料制品 防止水的污染--提倡使用无磷洗衣粉 | |
| C. | 基本安全常识: 饮用假酒中毒--由甲醇引起 食用假盐中毒--由亚硝酸钠引起 | |
| D. | 生活中的一些做法: 除去衣服上的油污--可用汽油洗涤 使煤燃烧更旺--可增大煤与空气接触面积 |
9.把一套以液化石油气(主要成分为C3H8和C4H10)为燃料的炉灶,现改用天然气(主要成分为CH4)为燃料,需要调整进入炉灶的燃料和空气的量.正确方法为( )
| A. | 只需调大燃料气的进气量 | B. | 只需调大空气的进气量 | ||
| C. | 同时调大燃料气和空气的量 | D. | 同时调小燃料气和空气的量 |
16.可持续发展观是科学发展观的核心内容.下列产品的使用符合可持续发展观的是( )
| A. | 含磷洗涤剂 | B. | 氟利昂 | C. | 乙醇汽油 | D. | 镍镉电池 |
10.下列个反应中,符合如图所示能量变化的是( )
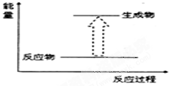

| A. | 乙醇与水反应 | |
| B. | 氧化钙与水反应 | |
| C. | 甲烷在氧气中燃烧 | |
| D. | 氢氧化钡晶体[Ba(OH)2•8H2O]与氯化铵晶体混合反应 |
11.下列变化不需要破坏化学键的是( )
| A. | 加热氯化铵 | B. | 氯化氢溶于水 | ||
| C. | 液态水变为水蒸气 | D. | 氯化钠熔化 |
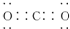 ;
; ;
;