题目内容
【题目】氯气是一种重要的化工原料,在生活和生产中的应用十分广泛。请回答:
(1)在工业上,“氯碱工业”是生产氯气的主要方法。请写出工业制备氯气的离子方程式____。
(2)实验室常用MnO2与浓盐酸反应制备Cl2,装置如图所示:
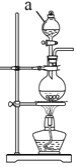
仪器a的名称为____。制备实验开始时,先检査装置气密性,接下来的操作依次是____(填序号)。
①往烧瓶中加入MnO2粉末 ②加热 ③往烧瓶中加入浓盐酸
(3)为证明Cl2与H2O反应为可逆反应,将生成的气体通入图所示装置:
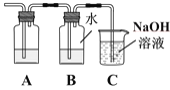
①装置A中应加入的试剂是____。
②证明可逆反应,需验证在B中反应物和生成物同时存在,证明氯水中有Cl2存在的现象是____,仅使用一种试剂证明氯水中HCl和HClO均存在,合适的试剂是____。
A.AgNO3溶液 B.石蕊试液 C.NaOH溶液 D.品红溶液
③装置C中NaOH溶液的作用是____。
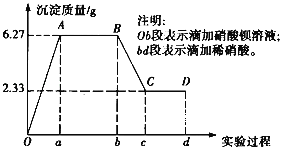
(4)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度(残余液体积已知)。甲同学提出下列具体方案。请你从下列实验方案中选择合理的实验方法____。
A.在残余液中加入足量AgNO3溶液,过滤,洗涤,干燥,称量沉淀的质量
B.在残余液中加入足量NaHCO3固体,将反应后的气体直接用碱石灰吸收,测定生成的气体的质量
C.在残余液中加入足量锌片,测量生成气体的体积,折算成标准状况下的体积
【答案】2Cl-+2H2O![]() Cl2↑+H2↑+2OH-分液漏斗①③②饱和食盐水装置B中的溶液呈黄绿色B尾气吸收C
Cl2↑+H2↑+2OH-分液漏斗①③②饱和食盐水装置B中的溶液呈黄绿色B尾气吸收C
【解析】
(1)电解饱和食盐水可以得到氢氧化钠、氯气和氢气,反应的方程式为2Cl-+2H2O![]() Cl2↑+H2↑+2OH-;
Cl2↑+H2↑+2OH-;
(2)仪器a的名称为分液漏斗,制备实验开始时,先检査装置气密性,接下来的操作依次是:检查装置气密性后,加药顺序一般是先加入固体药品,再加入液药品,最后再加热,因此正确的顺序是①③②;
(3)①生成的氯气中含有氯化氢,因此装置A中应加入的试剂为饱和食盐水,作用是用来除去氯气中的氯化氢;
②证明可逆反应,需验证在B中反应物和生成物同时存在,证明氯水中有Cl2存在的现象是装置B中的溶液呈黄绿色,仅使用一种试剂证明氯水中HCl和HClO均存在,利用盐酸的酸性和次氯酸的漂白性,合适的试剂是石蕊试液,先变红色后褪色证明氯化氢和次氯酸的存在,答案选B;
③氯气有毒,因此装置C中NaOH溶液的作用是尾气吸收;
(4)制备反应会因盐酸浓度下降而停止,为测定反应残余液中盐酸的浓度,则
A.在残余液中加入足量AgNO3溶液,过滤,洗涤,干燥,称量沉淀的质量,包含生成盐中氯离子生成的沉淀,不能测定反应残余液中盐酸的浓度,A错误;
B.在残余液中加入足量NaHCO3固体,将反应后的气体直接用碱石灰吸收,测定生成的气体的质量为二氧化碳和水蒸气的质量,不能测定反应残余液中盐酸的浓度,B错误;
C.在残余液中加入足量锌片,测量生成气体的体积,折算成标准状况下的体积,可以测定剩余盐酸的浓度,C正确;
答案选C。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案【题目】下列实验方案、现象、得出的结论均正确的是
选项 | 实验及现象 | 结论 |
A | 向SiO2固体加入过量盐酸振荡,固体不溶解 | SiO2不溶于任何酸 |
B | 用玻璃棒蘸取某样品进行焰色反应时观察到黄色火焰 | 该样品含钠元素 |
C | 向酸化的KMnO4溶液通入SO2,向反应后的溶液中加入BaCl2产生白色沉淀 | 白色沉淀为BaSO3 |
D | 将镁条点燃,迅速伸入集满CO2的集气瓶有白色固体和黑色颗粒产生 | CO2具有氧化性 |
A. A B. B C. C D. D
【题目】下列装置所示的实验中,不能达到实验目的是
|
|
|
|
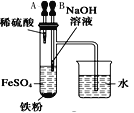
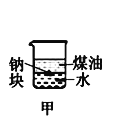
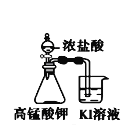
A.长时间看到Fe(OH)2白色沉淀 | B.证明ρ(煤油)< ρ(钠) < ρ(水) | C.探究氧化性: KMnO4>Cl2>I2 | D.比较NaHCO3、Na2CO3的热稳定性 |
A. A B. B C. C D. D
【题目】在80℃时,将0.4mol的四氧化二氮气体充入2L已抽空的固定容积的密闭容器中,隔一段时间对该容器内的物质进行分析,得到如下数据:反应进行至100s后将反应混合物的温度降低,发现气体的颜色变浅.
时间(s) c(mol/L) | 0 | 20 | 40 | 60 | 80 | 100 |
c(N2O4) | 0.20 | a | 0.10 | c | d | e |
c(NO2) | 0.00 | 0.12 | b | 0.22 | 0.22 | 0.22 |
(1)表中b_____c(填“<”、“=”、“>”).
(2)20s时,N2O4的浓度为_____mol/L,0~20s内N2O4的平均反应速率为_________.
(3)该反应在80℃时该反应的平衡常数K值为_______(保留2位小数).