题目内容
(16分)下图所示物质中(部分产物和反应条件未标出),只有A是单质,常温下B和C呈气态,且B是导致酸雨的大气污染物,W是淡黄色固体。
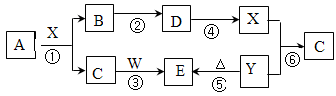
据此回答下列问题:
(1)物质W的名称为 ,由B生成D的化学方程式为 。
(2)请写出X和 Y反应的离子方程式: 。
(3)上图反应中不属于氧化还原反应的有 (填写序号)。
(4)写出A和X反应的化学方程式 ;若生成的B在标准状况下的体积为22.4L,则反应中转移电子数目为 。
(5)请写出C和W反应的化学方程式: 。在这个反应中生成1mol气体转移电子的物质的量为 。

据此回答下列问题:
(1)物质W的名称为 ,由B生成D的化学方程式为 。
(2)请写出X和 Y反应的离子方程式: 。
(3)上图反应中不属于氧化还原反应的有 (填写序号)。
(4)写出A和X反应的化学方程式 ;若生成的B在标准状况下的体积为22.4L,则反应中转移电子数目为 。
(5)请写出C和W反应的化学方程式: 。在这个反应中生成1mol气体转移电子的物质的量为 。
(共16分,每空2分)
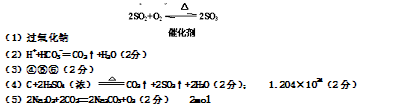

(1)物质W的名称为过氧化钠,由B生成D的化学方程式为:2SO2+O2 2SO3
2SO3
(2)X和 Y反应的离子方程式:H++HCO3-=H2O+CO2↑
(3)上图反应中不属于氧化还原反应的有:④⑤⑥
(4)A和X反应的化学方程式: C+2H2SO4(浓) CO2↑+2SO2↑+2H2O 反应中转移电子数目为1.204×1024
CO2↑+2SO2↑+2H2O 反应中转移电子数目为1.204×1024
(5)C和W反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑生成1mol气体转移电子的物质的量为2mol。
 2SO3
2SO3(2)X和 Y反应的离子方程式:H++HCO3-=H2O+CO2↑
(3)上图反应中不属于氧化还原反应的有:④⑤⑥
(4)A和X反应的化学方程式: C+2H2SO4(浓)
 CO2↑+2SO2↑+2H2O 反应中转移电子数目为1.204×1024
CO2↑+2SO2↑+2H2O 反应中转移电子数目为1.204×1024(5)C和W反应的化学方程式:2Na2O2+2CO2=2Na2CO3+O2↑生成1mol气体转移电子的物质的量为2mol。

练习册系列答案
 新活力总动员暑系列答案
新活力总动员暑系列答案 龙人图书快乐假期暑假作业郑州大学出版社系列答案
龙人图书快乐假期暑假作业郑州大学出版社系列答案
相关题目
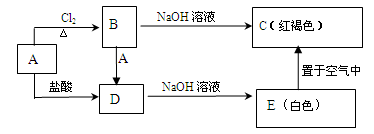
 ,该元素在周期表中的位置是
,该元素在周期表中的位置是