题目内容
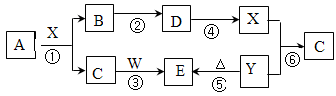
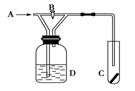
(6分) 现有A、B、C、D、E、F、G六种物质,已知,A、B、C、D是气体,A是密度最小的气体,B在通常情况下呈黄绿色,把四种气体分别通入酸性硝酸银溶液中,通入B、D气体时立即出现白色沉淀,纯净的A可以在B中安静地燃烧,发出苍白色的火焰并生成D。把无色无刺激性气味气体C通入澄清石灰水时变浑浊。E为常见的金属单质,其与D的水溶液发生反应产生A和F,F中通入B气体可以得到G
(1)D、F的化学式分别为:
D______________________ F_____________________
(2) C的电子式为 。
(3) B与F生成G的离子方程式为________________________________
(4) C与澄清石灰水反应的离子方程式为 。
(5)实验室用KSCN检验G中阳离子,现象是________________________
(1)D、F的化学式分别为:
D______________________ F_____________________
(2) C的电子式为 。
(3) B与F生成G的离子方程式为________________________________
(4) C与澄清石灰水反应的离子方程式为 。
(5)实验室用KSCN检验G中阳离子,现象是________________________
(每空1分,6分)
(1)HCl FeCl2 (2):O::C::O: (3)2Fe2++ Cl2 = 2Fe3++2 Cl-
(4) CO2+Ca2++2OH——=CaCO3↓+H2O (5)出现血红色溶液
(1)HCl FeCl2 (2):O::C::O: (3)2Fe2++ Cl2 = 2Fe3++2 Cl-
(4) CO2+Ca2++2OH——=CaCO3↓+H2O (5)出现血红色溶液
由题意可知:A 为氢气;B 为氯气;C 为二氧化碳;D为氯化氢;E为铁;F为氯化亚铁;G是氯化铁。
(1)D、F的化学式分别为:HCl FeCl2
(2) C的电子式为):O::C::O:
(3) B与F生成G的离子方程式为:2Fe2++ Cl2 = 2Fe3++2 Cl-
(4) C与澄清石灰水反应的离子方程式为:CO2+Ca2++2OH-=CaCO3↓+H2O
(5)实验室用KSCN检验G中阳离子,现象是溶液出现血红色。
(1)D、F的化学式分别为:HCl FeCl2
(2) C的电子式为):O::C::O:
(3) B与F生成G的离子方程式为:2Fe2++ Cl2 = 2Fe3++2 Cl-
(4) C与澄清石灰水反应的离子方程式为:CO2+Ca2++2OH-=CaCO3↓+H2O
(5)实验室用KSCN检验G中阳离子,现象是溶液出现血红色。

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
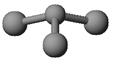
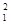 H原子中的中子和质子
H原子中的中子和质子