题目内容
5.下列实验能达到实验目的是ADEF.A.用硫酸铜溶液除去电石与水反应生成的乙炔气体中的杂质
B.溴乙烷与NaOH水溶液混合共热一段时间后,向水层加入AgNO3溶液,观察到淡黄色沉淀产生.
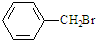
C.甲苯与液溴混合,加入少量铁屑,制备
D.已知3.0mol•L-1 CuSO4溶液中Cu2+开始沉淀的pH为4,Fe3+完全沉淀时溶液的pH为3.3,则可以用氧化铜除去该溶液中含有的杂质Fe3+
E.只用FeCl3溶液就可以鉴别出苯酚溶液、NaOH溶液、KHCO3溶液、苯、溴乙烷五种无色液体
F.用稀盐酸和溴的四氯化碳溶液可证明1-溴戊烷在NaOH水溶液与NaOH醇溶液中发生的反应类型不同
G.通过石油的分馏可以直接得到甲烷、乙烯和苯等产品.
分析 A.电石和水反应生成的乙炔气体中的杂质有硫化氢以及磷化氢等;
B.溴乙烷与NaOH水溶液混合共热一段时间后,先加稀硝酸中和未反应的碱;
C.甲苯与液溴混合,加入少量铁屑,苯环上氢原子被溴原子取代;
D.铜离子和铁离子完全沉淀需要的pH不同,可以用CuO调节溶液的pH,从而除去铁离子;
E.氯化铁溶液苯酚溶液混合产生显色反应、和NaOH溶液生成红褐色沉淀、和KHCO3溶液发生双水解反应生成沉淀和气体、和苯混合分层且苯在上层、和溴乙烷混合分层且水在上层;
F.1-溴戊烷在NaOH水溶液与NaOH醇溶液中分别发生取代反应和消去反应,分别生成醇和烯烃,烯烃和溴发生加成反应,醇和溴不反应;
G.通过石油的催化裂化可以直接得到甲烷、乙烯.
解答 解:A.CuSO4和H2S可以反应生成黑色的CuS沉淀,硫酸铜具有较强的氧化性,可以将磷化氢氧化而除去,故A正确;
B.溴乙烷在碱性条件下水解,检验是否生成溴离子,在水解液中加入硝酸酸化,排除AgOH的干扰,溴化银是淡黄色沉淀,故B错误;
C.甲苯与液溴混合,加入少量铁屑,苯环上氢原子被溴原子取代,所以不能得到 ,故C错误;
,故C错误;
D.铜离子和铁离子完全沉淀需要的pH不同,可以用CuO调节溶液的pH,从而除去铁离子且不引进杂质,故正确;
E.氯化铁溶液苯酚溶液混合产生显色反应、和NaOH溶液生成红褐色沉淀、和KHCO3溶液发生双水解反应生成沉淀和气体、和苯混合分层且苯在上层、和溴乙烷混合分层且水在上层,反应现象不同,可以鉴别,故正确;
F.1-溴戊烷在NaOH水溶液与NaOH醇溶液中分别发生取代反应和消去反应,分别生成醇和烯烃,烯烃和溴发生加成反应,醇和溴不反应,反应现象不同,可以鉴别,故正确;
G.通过石油的催化裂化可以直接得到甲烷、乙烯,故错误.
故选ADEF.
点评 本题考查化学实验方案评价,为高频考点,涉及物质制备、物质鉴别、官能团的检验、除杂等知识点,明确物质的性质及实验原理是解本题关键,注意反应物相同但条件不同其产物不同,题目难度中等.

| A. | HCl溶于水 | B. | 干冰升华 | ||
| C. | 固体NaCl熔融 | D. | 煤矿中瓦斯(主要成分CH4)遇火爆炸 |
| A. | FeCl3溶液 | B. | 溴水 | ||
| C. | 酸性高锰酸钾溶液 | D. | NaOH溶液 |
| A. | 苯甲酸的重结晶实验中要得到纯净的苯甲酸固体需要进行两次过滤操作 | |
| B. | 实验室制乙烯时,为减弱浓硫酸对有机物的碳化作用,应用小火缓慢加热 | |
| C. | 在石油的分馏、制硝基苯、制乙烯的实验中,都要使温度计的水银液泡浸入反应液中,以控制实验温度 | |
| D. | 制备硝基苯,混合药品的顺序为:向试管中先加入苯,再加入浓硫酸,最后加入浓硝酸 |
| A. | 化学式为CF2Cl2的物质可以看作是甲烷的衍生物,它有两种分子结构 | |
| B. | 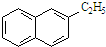 所有原子都处于同一平面 所有原子都处于同一平面 | |
| C. | C3H8O有2种同分异构体 | |
| D. | 甲苯的二氯代物共有10种 |
| A. | Ca(HCO3)2 | B. | NaHCO3 | C. | Na2CO3 | D. | CaCO3 |
| A. | 铝原子的结构示意图: | B. | 乙炔的比例模型: | ||
| C. | 水分子的电子式: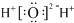 | D. | 硝基苯的结构简式: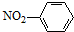 |
| A. | 澄清溶液:Fe3+、NH4+、Cl-、ClO- | |
| B. | pH=1的溶液:Na+、Mg2+、Ca2+、NO3- | |
| C. | 滴加酚酞显红色的溶液:K+、Cl-、Br-、HCO3- | |
| D. | 亚硫酸钠溶液:K+、SO42-、NO3-、H+ |
| A. | 用25mL量筒量取4.0 mol/L的盐酸5.62 mL | |
| B. | 用托盘天平称取5.85 g NaCl固体 | |
| C. | 用蒸发方法使NaCl从溶液中析出时,将蒸发皿中NaCl 溶液全部加热蒸干 | |
| D. | 用500 mL容量瓶可配制450 mL 0.2mol/L H2SO4溶液 |