题目内容
【题目】下列说法正确的是
A. 反应2H2(g)+O2(g)=2H2O(l) 在室温下可自发进行,则该反应的△H<0
B. 常温常压下,7.8gNa2O2与水完全反应,产生1.12L气体
C. 煤的干馏是物理变化,石油的裂化是化学变化
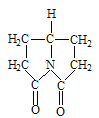
D. 气体分子总数不再改变时,反应H2(g)+I2(g)![]() 2HI(g))达到平衡
2HI(g))达到平衡
【答案】A
【解析】A、反应2H2(g)+O2(g)=2H2O(l) 在室温下可自发进行,△H-T△S<0,因为反应气体分子数减少,△S<0,则该反应的△H<0,故选A;B、7.8gNa2O2与水完全反应,在标准状况产生1.12L气体,故B错误;C、煤的干馏是指煤在隔绝空气的条件下加热,生成煤焦油、焦炭、焦炉煤气等物质,属于化学变化;石油分馏是指通过石油中含有的物质的沸点不同而使各种物质分离开的一种方法,该过程中没有新物质生成,属于物理变化;从重质油生产汽油和柴油的过程称为裂化;而把从轻质油生产小分子烯烃和芳香烃的过程称为裂解,石油的裂化和裂解,是化学变化,故C错误;D、H2(g)+I2(g)![]() 2HI(g))是反应前后气体体积不变的反应,气体分子总数不再改变时,不能说明反应达到平衡,故D错误;故选A。
2HI(g))是反应前后气体体积不变的反应,气体分子总数不再改变时,不能说明反应达到平衡,故D错误;故选A。

【题目】某课外小组设计的实验室制取乙酸乙酯的装置如图1:
己知:A中放有浓硫酸;B中放有9.5mL无水乙醇和6mL冰醋酸;D中放有饱和碳酸钠溶液

有关有机物的沸点.
试剂 | 乙醚 | 乙醇 | 乙酸 | 乙酸乙酯 |
沸点/℃ | 34.7 | 78.5 | 118 | 77.1 |
请回答:
(1)若用同位素18O示踪法确定反应产物水分子中氧原子的提供者,写出能表示18O位置的化学方程式:___________________________
(2)实验过程中滴加大约3mL浓硫酸,B的容积最合适的是_______
A.25mL B.50mL C.250mL D.500mL
(3)在步骤①④中都用到沸石防暴沸,下列关于沸石的说法正确的是___
A.实验室沸石也可用碎瓷片等代替
B.如果忘加沸石,可速将沸石加至将近沸腾的液体中
C.当重新进行蒸馏时,用过的沸石可继续使用
D.沸石为多孔性物质,可使液体平稳地沸腾
(4)浓硫酸的作用:催化剂和________; 反应中加入过量的乙醇,目的是_____.
(5)仪器C的名称是____,其作用有冷凝乙酸乙酯和_____,若反应前向D中加入几滴酚酞,溶液呈红色.实验完毕后,将烧杯D中的溶液充分振荡、静止,现象为_____.
(6)现拟分离乙酸乙酯(含少量乙醇和乙酸)粗产品,如图2是分离操作步骤流程图:
则试剂a是:_____,试剂b是:_____.分离方法I是_____,分离方法II是____.
(7)甲、乙两位同学欲将所得含有乙醇、乙酸和水的乙酸乙酯粗产品提纯,在未用指示剂的情况下,他们都先加NaOH溶液中和酯中过量的酸,然后用蒸馏水将酯分离出来.甲、乙两人实验结果如下:甲得到了显酸性的酯的混合物;乙得到了大量水溶性的物质;丙同学分析了上述实验目标产物后认为甲、乙的实验没有成功.试解答下列问题:
①甲实验失败的原因是:________.②乙实验失败的原因是:________.