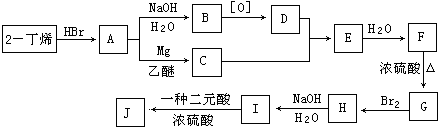
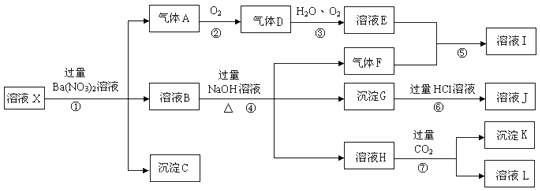
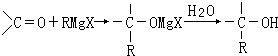题目内容
【题目】欲配制100mL 1.0mol/L Na2CO3溶液,正确的方法是( )
①将10.6g Na2CO3溶于100mL水中
②将28.6g Na2CO310H2O溶于少量水中,再用水稀释至100mL
③将20ml 5.0mol/L Na2CO3溶液用水稀释至100mL.
A.①②
B.②③
C.只有②
D.只有③
【答案】B
【解析】①10.6g Na2CO3的物质的量n(Na2CO3)= ![]() =0.1mol,溶液的体积不等于溶剂的体积,所以无法计算出Na2CO3溶液的物质的量浓度,故①不符合题意;
=0.1mol,溶液的体积不等于溶剂的体积,所以无法计算出Na2CO3溶液的物质的量浓度,故①不符合题意;
②28.6g Na2CO310H2O的物质的量n( Na2CO310H2O)= ![]() =0.1mol,则n(Na2CO3)=n( Na2CO310H2O)=0.1mol,Na2CO3溶液的物质的量浓度为
=0.1mol,则n(Na2CO3)=n( Na2CO310H2O)=0.1mol,Na2CO3溶液的物质的量浓度为 ![]() =1mol/L,故②符合题意;
=1mol/L,故②符合题意;
③溶液稀释前后溶质的物质的量不变,设稀释后溶液浓度为C,则20ml×5.0mol/L=100mL×C,解得C=1.0mol/L,故③符合题意;
所以答案是:B;
【考点精析】根据题目的已知条件,利用配制一定物质的量浓度的溶液的相关知识可以得到问题的答案,需要掌握配制物质的量浓度溶液时,先用烧杯加蒸馏水至容量瓶刻度线1cm~2cm后,再改用交投滴管加水至刻度线.

练习册系列答案
 优等生题库系列答案
优等生题库系列答案
相关题目