题目内容
【题目】H2O2是生产、生活、实验中常用的试剂。
I.工业上制备H2O2的流程如下:
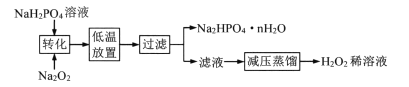
(1)“转化”中反应的化学方程式为_________:“低温放置”的目的是_________
(2)图甲为“减压蒸馏”的部分装置,该装置由克氏蒸馏头和_________(填仪器名称)组成。
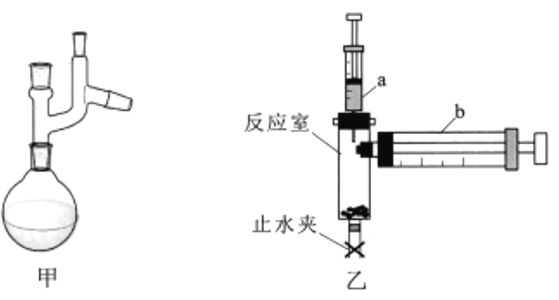
lI.实验小组利用图乙装置测定阿伏加德罗常数(NA)
(3)实验准备
①H2O2溶液浓度标定。可选用_________(填标号)试剂对H2O2溶液进行滴定,测定其浓度。
A.H2C2O4B.KMnO4C.淀粉KI
②装置气密性检查。打开止水夹,将注射器b的活塞推至底部,拉动注射器a活塞吸入10mL空气,关闭止水夹。向下推动注射器a活塞至底,当观察到注射器b的现象为_________,说明装置的气密性良好。
(4)测定过程
①在反应室中加入适量MnO2,将注射器b活塞推至底部,关闭止水夹。用注射器a准确抽取cmol/LH2O2溶液VlmL,缓慢地注入反应室后,固定注射器a活塞。
②反应结束后,待反应体系处于_________状态时,读取注射器b的气体体积为V2mL,则产生O2的体积为____mL。
③设室温下O2的密度为ρg/L,一个O2实际质量为mg,则NA=____(用含ρ等字母的代数式表示)。
(5)该实验利用H2O2作为生氧剂的优点有_________(写两条)。
【答案】Na2O2+2NaH2PO4=2Na2HPO4+H2O2 防止H2O2受热分解,沉降Na2HPO4·nH2O固体 圆底烧瓶 B 注射器b的活塞向右移动,且最终注射器b中的气体体积为10mL 恢复室温或体积不再改变或压强不再改变 V2-V1 ![]() 反应完全、无污染、反应速率快等合理答案均可
反应完全、无污染、反应速率快等合理答案均可
【解析】
由反应流程可知转化方程式为Na2O2+2NaH2PO4=2Na2HPO4+H2O2,H2O2 受热易分解为水和氧气,故应低温放置;
H2O2具有还原性,与KMnO4反应现象明显,可以利用溶液颜色变化来测定H2O2溶液浓度,
由分析可知:
(1)转化中方程式为Na2O2+2NaH2PO4=2Na2HPO4+H2O2,低温放置目的在于防止H2O2受热分解,沉降Na2HPO4·nH2O固体;
(2)由装置图可知反应中的仪器为圆底烧瓶;
(3)①由H2O2的还原性,以及溶液颜色的变化作为实验结束标志可知选用KMnO4溶液测量结果更精确,故选B;
②注射器b的活塞向右移动,且最终注射器b中的气体体积为10mL
(4)①测量气体体积时应避免温度对气体体积的影响,准确测量气体体积应在室温下,故答案为:恢复室温或体积不再改变或压强不再改变;
②注射器中气体体积的变化是由于H2O2的分解产生的O2引起的,故氧气的体积为V2-V1 mL;
③由题中信息可知生成的![]() 的质量m(O2)=ρg/L
的质量m(O2)=ρg/L![]() L,由
L,由![]() 可知:
可知:![]() ;故可得m(O2)=
;故可得m(O2)=![]() 所以结合式子可得NA=
所以结合式子可得NA=![]() ;
;
(5)![]() 作为自身具有氧化性,反应产物为水和氧气,故本实验的优点是反应完全、无污染、反应速率快等。
作为自身具有氧化性,反应产物为水和氧气,故本实验的优点是反应完全、无污染、反应速率快等。