题目内容
已知:T℃、P kpa时,容积为V 的密闭容器中充有1molA和2molB,保持恒温恒压使反应达平衡:A(g)+B(g)?C(g),平衡时C 的体积分数为40%.
(1)欲保持温度、压强在上述条件下不变,在密闭容器中充入2molA和4molB,则平衡时体系容积为 ,C的体积分数为 .
(2)另取一个容积固定不变的密闭容器,仍控制温度为T℃,加入1molB和1molC,要使平衡时C 的体积分数仍为40%,则该密闭容器体积为 .
(1)欲保持温度、压强在上述条件下不变,在密闭容器中充入2molA和4molB,则平衡时体系容积为
(2)另取一个容积固定不变的密闭容器,仍控制温度为T℃,加入1molB和1molC,要使平衡时C 的体积分数仍为40%,则该密闭容器体积为
考点:化学平衡的计算
专题:化学平衡专题
分析:恒温恒压,使反应:A(g)+B(g) ?C(g)达到平衡时,C的物质的量分数为40%,
?C(g)达到平衡时,C的物质的量分数为40%,
(1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同,
令转化的物质的量为a,则:
A(g)+B(g) ?C(g)
?C(g)
开始(mol):1 2 0
变化(mol):a a a
平衡(mol):(1-a ) (2-a) a
则
×100%=40%,解得a=
mol,故平衡后反应混合物的总的物质的量为3mol-
mol=
mol,
利用同温同压下体积之比等于物质的量之比,计算容器的体积,由于是恒压过程,起始反应物成比例,所以C的体积分数和原平衡一样,据此答题;
(2)容积固定不变的密闭容器,仍然控制温度为T K,使1mol A和1mol B反应达到平衡状态时,C的物质的量分数仍然为40%,则
A(g)+B(g) ?C(g)
?C(g)
开始 1 1 0
转化 x x x
平衡 1-x 1-x x
则
=40%,解得x=
,利用同温同压下体积之比等于物质的量之比,计算容器的体积.
 ?C(g)达到平衡时,C的物质的量分数为40%,
?C(g)达到平衡时,C的物质的量分数为40%,(1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同,
令转化的物质的量为a,则:
A(g)+B(g)
 ?C(g)
?C(g)开始(mol):1 2 0
变化(mol):a a a
平衡(mol):(1-a ) (2-a) a
则
| a |
| 3-a |
| 6 |
| 7 |
| 6 |
| 7 |
| 15 |
| 7 |
利用同温同压下体积之比等于物质的量之比,计算容器的体积,由于是恒压过程,起始反应物成比例,所以C的体积分数和原平衡一样,据此答题;
(2)容积固定不变的密闭容器,仍然控制温度为T K,使1mol A和1mol B反应达到平衡状态时,C的物质的量分数仍然为40%,则
A(g)+B(g)
 ?C(g)
?C(g)开始 1 1 0
转化 x x x
平衡 1-x 1-x x
则
| x |
| 1-x+1-x+x |
| 4 |
| 7 |
解答:
解:恒温恒压,使反应:A(g)+B(g) ?C(g)达到平衡时,C的物质的量分数为40%,
?C(g)达到平衡时,C的物质的量分数为40%,
(1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同,
令转化的物质的量为a,则:
A(g)+B(g) ?C(g)
?C(g)
开始(mol):1 2 0
变化(mol):a a a
平衡(mol):(1-a ) (2-a) a
则
×100%=40%,解得a=
mol,故平衡后反应混合物的总的物质的量为3mol-
mol=
mol,
由于是恒压过程,起始反应物成比例,所以在容器中充入2molA和4molB和容器中充有1molA和2molB时C的体积分数一样仍为40%,所以在密闭容器中充入2molA和4molB,则平衡时体系的总物质的量为
mol,由同温同压下体积之比等于物质的量之比,则容器的体积VL×
mol×
=
VL,
故答案为:
VL;40%;
(2)容积固定不变的密闭容器,仍然控制温度为T K,使1mol A和1mol B反应达到平衡状态时,C的物质的量分数仍然为40%,则
A(g)+B(g) ?C(g)
?C(g)
开始(mol):1 1 0
变化(mol):x x x
平衡(mol):(1-x ) (1-x) x
则
=40%,解得x=
,由同温同压下体积之比等于物质的量之比,则容器的体积为VL×
=
VL,故答案为:
VL.
 ?C(g)达到平衡时,C的物质的量分数为40%,
?C(g)达到平衡时,C的物质的量分数为40%,(1)温度和压强在上述条件下恒定不变,在密闭容器中充入2mol A和2mol B,2mol:2mol=1mol:1mol,平衡等效,平衡时体积分数与原状态达平衡的体积分数相同,
令转化的物质的量为a,则:
A(g)+B(g)
 ?C(g)
?C(g)开始(mol):1 2 0
变化(mol):a a a
平衡(mol):(1-a ) (2-a) a
则
| a |
| 3-a |
| 6 |
| 7 |
| 6 |
| 7 |
| 15 |
| 7 |
由于是恒压过程,起始反应物成比例,所以在容器中充入2molA和4molB和容器中充有1molA和2molB时C的体积分数一样仍为40%,所以在密闭容器中充入2molA和4molB,则平衡时体系的总物质的量为
| 30 |
| 7 |
| 30 |
| 7 |
| 1 |
| 3 |
| 10 |
| 7 |
故答案为:
| 10 |
| 7 |
(2)容积固定不变的密闭容器,仍然控制温度为T K,使1mol A和1mol B反应达到平衡状态时,C的物质的量分数仍然为40%,则
A(g)+B(g)
 ?C(g)
?C(g)开始(mol):1 1 0
变化(mol):x x x
平衡(mol):(1-x ) (1-x) x
则
| x |
| 1-x+1-x+x |
| 4 |
| 7 |
2mol-
| ||
| 2mol |
| 5 |
| 7 |
| 5 |
| 7 |
点评:本题考查化学平衡的有关计算、等效平衡等,题目难度中等,注意对等效平衡的理解,掌握等效平衡规律即可解答.

练习册系列答案
相关题目
下列金属材料中,最适合制造飞机外壳的是( )
| A、镁铝合金 | B、铜合金 |
| C、碳素钢 | D、钠钾合金 |
一定条件下存在反应:A(g)+B(g)?C(g)+D(g)△H<0.现有三个相同的2L恒容绝热(与外界没有热量交换)密闭容器Ⅰ、Ⅱ、Ⅲ,在Ⅰ中充入1mol A和1mol B,在Ⅱ中充入1mol C和1mol D,在Ⅲ中充入2mol A和2mol B,500℃条件下开始反应.达到平衡时,下列说法正确的是( )
| A、容器Ⅰ、Ⅱ中正反应速率相同 |
| B、容器Ⅰ、Ⅲ中反应的平衡常数相同 |
| C、容器Ⅰ中A的物质的量比容器Ⅱ中的多 |
| D、容器Ⅰ中A的转化率与容器Ⅱ中C的转化率之和小于1 |
下列说法正确的是( )
| A、原子晶体中只存在非极性共价键 |
| B、稀有气体形成的晶体属于分子晶体 |
| C、干冰升华时,分子内共价键会发生断裂 |
| D、金属元素和非金属元素形成的化合物一定是离子化合物 |
0.1mol某金属和足量盐酸反应,产生0.15mol H2,该金属的核电荷数是( )
| A、11 | B、12 | C、13 | D、19 |
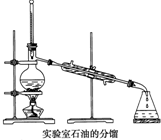 实验室中常采用如图所示装置进行石油分馏,请回答下列问题:
实验室中常采用如图所示装置进行石油分馏,请回答下列问题: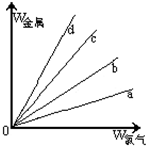
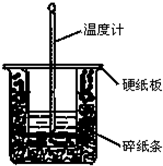 50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题:
50mL 0.50mol?L-1盐酸与50mL 0.55mol?L-1NaOH溶液在图示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: