题目内容
7.资料显示:“氨气可在纯氧中安静燃烧…某校化学小组学生设计如下装置(图中铁夹等夹持装置已略去)进行氨气与氧气在不同条件下反应的实验.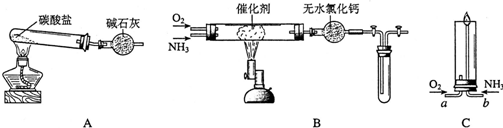
(1)用装置A制取纯净、干燥的氨气,大试管内碳酸盐的化学式是(NH4)2CO3或NH4HCO3;碱石灰的作用是吸收水和二氧化碳.
(2)将产生的氨气与过量的氧气通到装置B(催化剂为铂石棉)中,用酒精喷灯加热:
①氨催化氧化的化学方程式是4NH3+5O2 $\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O试管内气体变为红棕色,该反应的化学方程式是2NO+O2=2NO2
②停止反应后,立即关闭B中两个活塞.一段时间后,将试管浸入冰水中.试管内气体颜色变浅,请结合化学方程式说明原因2NO2?N2O4 △H<0,降温平衡向正反应方向移动,颜色变浅
(3)将过量的氧气与A产生的氨气分别从a、b两管进气口通人到装置C中,并在b管上端点燃氨气,两气体通入的先后顺序是:先通入O2(O2,NH3 ),后通入NH3(O2,NH3)其理由是如果先通入NH3,NH3在空气中不能点燃,NH3逸出会造成污染.
分析 (1)碳酸盐加热分解能产生NH3,只有(NH4)2CO3或NH4HCO3,碱石灰可以吸收酸性气体,并用于干燥氨气;
(2)①氨气在催化剂作用下反应生成一氧化氮和水;一氧化氮不稳定,容易与空气中的氧气反应生成红棕色的二氧化氮;
②由于2NO2(g)?N2O4(g);△H<0,正反应为放热反应,当温度降低时,平衡向正反应方向移动,依次进行判断;
(3)若先通入NH3,NH3在空气中不能点燃,可在纯氧中安静燃烧,依次进行判断;
解答 解:(1)碳酸盐加热分解能产生NH3,只有(NH4)2CO3或NH4HCO3,碱石灰可以吸收酸性气体,并用于干燥氨气,所以碱石灰的作用:吸收水和二氧化碳;
故答案为:(NH4)2CO3或NH4HCO3;吸收水和二氧化碳;
(2)①氨气在催化剂作用下反应生成一氧化氮和水,4NH3+5O2 $\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O;一氧化氮与氧气反应生成二氧化氮,方程式:2NO+O2=2NO2;
故答案为:4NH3+5O2 $\frac{\underline{\;催化剂\;}}{△}$4NO+6H2O;2NO+O2=2NO2;
②将试管浸入冰水中,由于2NO2(g)?N2O4(g)△H<0,正反应为放热反应,当温度降低时,平衡向正反应方向移动,部分红棕色的NO2转化为无色N2O4,故颜色变浅.
故答案为:2NO2?N2O4 △H<0,降温平衡向正反应方向移动,部分红棕色的NO2转化为无色N2O4;
(3)由于装置C上端开口,要点燃NH3,须先通入O2,后通入NH3,因为若先通入NH3,NH3在空气中不能点燃,NH3逸出会造成污染;
故答案为:O2;NH3;如果先通入NH3,NH3在空气中不能点燃,NH3逸出会造成污染.
点评 本题考查了氨气的制备和性质,熟悉制备原理和氨气性质是解题关键,题目难度不大.

| A. | 1mol | B. | 3mol | C. | 4mol | D. | 6mol |
| A | B |
| ①能使溴的四氯化碳溶液褪色; ②比例模型为:  ③能与水在一定条件下反应 | ①由C、H两种元素组成; ②球棍模型为: 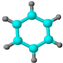 |
①A与溴的四氯化碳溶液反应的生成物的名称是1,2-二溴乙烷;写出在一定条件下,A生成高分子化合物的化学反应方程式
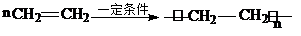 .
.②A与氢气发生加成反应后生成分子C,与C在分子组成和结构上相似的有机物有一大类(俗称“同系物”),它们均符合通式CnH2n+2.当n=4时,这类有机物开始出现同分异构体.
③B具有的性质是bc(填序号)
a.无色无味液体 b.有毒 c.不溶于水 d.密度比水大
e.能使酸性KMnO4溶液和溴水褪色 f.任何条件下不与氢气反应
写出在浓硫酸作用下,B与浓硝酸反应的化学方程式:C6H6+HNO3$→_{△}^{浓硫酸}$C6H5NO2+H2O.
(2)二恶英是严重的污染物,很难降解,毒性极大,它常由焚烧垃圾产生,其中一种异构体为
 ,它的分子式为C12H4Cl4,它是属于芳香族化合物(填“是”或“否”)
,它的分子式为C12H4Cl4,它是属于芳香族化合物(填“是”或“否”) 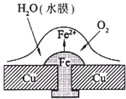 已知铅蓄电池的总反应PbO2+Pb+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )
已知铅蓄电池的总反应PbO2+Pb+2H2SO4 $?_{充电}^{放电}$ 2PbSO4+2H2O,图为铁铆钉铆在铜板上,有关叙述不正确的是( )| A. | 铅蓄电池放电时,电路中每转移2mol电子,生成1mol硫酸铅 | |
| B. | 如图,铁铆钉发生吸氧腐蚀,在铁钉附近滴加K3[Fe(CN)6]溶液,可观察铁钉附近有蓝色沉淀产生 | |
| C. | 铅蓄电池充电时,阳极电极反应为 PbSO4+2H2O-2e-═PbO2+4H++SO42- | |
| D. | 铅蓄电池放电时,内电路硫酸根离子向铅极移动,正极附近溶液的pH增大 |
| A. | 可用丁达尔现象区分溶液与胶体 | |
| B. | 胶体粒子直径在1 nm~100 nm之间 | |
| C. | 胶体粒子可以透过滤纸,不能透过半透膜 | |
| D. | 胶体带电荷,而溶液呈电中性 |

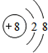 ;
;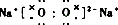 .
.