��Ŀ����
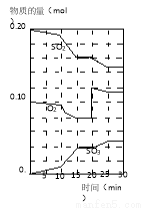
ij�¶��£��ܱ�������X��Y��Z��W��������ij�ʼŨ�Ⱥ�ƽ��Ũ�����±�������˵���������
���� | X | Y | Z | W |
��ʼŨ��/mol��L-1 | 0.5 | 0.6 | 0 | 0 |
ƽ��Ũ��/mol��L-1 | 0.1 | 0.1 | 0.4 | 0.6 |
A����Ӧ�ﵽƽ��ʱ��X��ת����Ϊ80%
B���÷�Ӧ��ƽ�ⳣ������ʽΪK=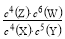
C������ѹǿ��ƽ�ⳣ�����䣬��ʹƽ��������Z�ķ����ƶ�
D���ı��¶ȿ��Ըı�˷�Ӧ��ƽ�ⳣ��
C
��������
���������A���ɱ������ݿ�֪��ƽ��ʱX��Ũ�ȱ仯��Ϊ0.5mol/L-0.1mol/L=0.4mol/L����X��ת����Ϊ0.4/0.5��100%=80%����A��ȷ��B���ɱ������ݿ�֪��ƽ��ʱ��c��X��=0.4mol/L����c��Y��=0.6mol/L-0.1mol/L=0.5mol/L����c��Z��=0.4mol/L����c��W��=0.6mol/L����X��Y��Z��W�Ļ�ѧ������֮��Ϊ0.4��0.5��0.4��0.6=4��5��4��6���ʷ�Ӧ����ʽΪ��4X��g��+5Y��g��?4Z��g��+6W��g�����ʸ÷�Ӧ�Ļ�ѧƽ�ⳣ��k=c4(Z)?c6(W)/c4(X)?c5(Y)����B��ȷ��C��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶Ȳ��䣬ƽ�ⳣ�����䣬������ѹǿƽ�ⳣ�����䣬��B�з�����֪����ӦΪ4X��g��+5Y��g��?4Z��g��+6W��g�����÷�Ӧ����Ӧ�������������Ӧ������ѹǿƽ�����淴Ӧ�ƶ�����C����D��ƽ�ⳣ��ֻ���¶�Ӱ�죬�¶ȸı䣬ƽ�ⳣ��һ���ı䣬��D��ȷ��
���㣺���黯ѧƽ�ⳣ����Ӱ�����ء���ѧƽ����йؼ����

��1������������ ��Cu����Һ̬SO2����CH3COOH����NaHCO3����H2O��������NaCl����BaSO4 ����������ʵ��� ������ţ�
��2�������£�0.1 mol��L-1NaHCO3��Һ��pH����8������Һ��Na����HCO3�D��CO32�D��OH�D ��������Ũ���ɴ�С��˳��Ϊ�� ��NaHCO3ˮ������ӷ���ʽ ��
��3������������ijһԪ��HA��NaOH��Һ����������������Һ��Ũ�Ⱥͻ�Ϻ�������Һ��pH���±���
ʵ���� | HA���ʵ���Ũ��(mol��L-1) | NaOH���ʵ���Ũ��(mol��L-1) | �����Һ ��pH |
a | 0.1 | 0.1 | pH��9 |
b | c | 0.2 | pH��7 |
��ش�
����a����������� HA��ǿ�ỹ������ ��
��b�����������c 0.2 (ѡ��������������С������ ��������)�������Һ������Ũ��c(A��)_______ c(Na��)��(ѡ��������������С������ ��������)
�� a��ʵ�����û����Һ����ˮ�������c(OH��)�� mol��L��1��