题目内容
氯碱工业常利用阳离子交换膜电解食盐水,下列说法不正确的是
| A.随着电解的进行,c(NaCl)降低,需不断补充饱和食盐水 |
| B.电解过程中采用增大阳极区溶液pH的方法,可以减少Cl2在水中的溶解量 |
| C.阳离子交换膜的作用是阻止OH-移向阳极,以使氢氧化钠在阴极区富集 |
| D.阳极表面用钛氧化物涂层处理,目的是降低电解产物Cl2对电极的腐蚀 |
B
解析

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有一合金由X、Y、Z、W四种金属组成,若将合金放入盐酸中只有Z、Y能溶解;若将合金置于潮湿空气中,表面只出现Z的化合物;若将该合金做阳极,用X盐溶液作电解液,通电时四种金属都以离子形式进入溶液中,但在阴极上只析出X。这四种金属的活动性顺序是 ( )
| A.Y>Z>W>X | B.Z>Y>W>X | C.W>Z>Y>X | D.X>Y>Z>W |
下列叙述中,正确的是
①锌跟稀硫酸反应制取氢气,加入少量CuSO4溶液能提高反应速率 ②镀层破损后,白铁(镀锌的铁)比马口铁(铁锡的铁)更易腐蚀; ③电镀时应把镀件置于电解槽的阴极 ;④冶炼铝时,把氧化铝加热成为熔融体后电解 ⑤钢铁表面常易腐蚀生成Fe2O3·nH2O
| A.①②③④⑤ | B.①③④⑤ | C.①③⑤ | D.②④ |
有关下列装置的叙述不正确的是

| A.图①铝片发生的电极反应式是:Al+4OH--3e-===AlO2-+2H2O |
| B.图②发生析氢腐蚀,离子反应方程式为:Fe+2H+===Fe2++H2↑ |
| C.图③溶液中发生了变化:4Fe(OH)2+O2+2H2O===4Fe(OH)3 |
| D.图④充电时,阳极反应是:PbSO4+2H2O-2e-===PbO2+SO42-+4H+ |
下列陈述和判断均正确,且有因果关系的是
| 选项 | 陈述 | 判断 |
| A | Si有良好的半导体性能 | Si可用于制备光导纤维 |
| B | 在未知溶液中加入稀硝酸和氯化钡溶液有沉淀生成 | 说明该未知溶液含有SO42- |
| C | 铁、铜、汞、银的金属活动性顺序为Fe>(H)>Cu>Hg>Ag | 要从矿石中冶炼得到金属单质,铁和铜必须用还原剂,汞和银只需加热 |
| D | 锌锰干电池碳棒是正极,MnO2是氧化剂 | 锌锰干电池是二次电池,可以反复充电 |
按下图的装置进行试验,若图中X轴表示阴极的电子的量,则Y轴可能表示为( )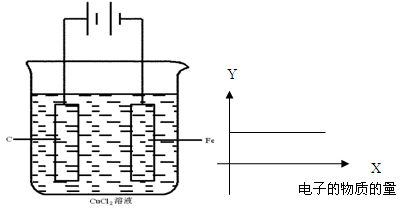
| A.Cu2+物质的量浓度 | B.C棒的质量 |
| C.Fe棒的质量 | D.Cl-物质的量浓度 |
下列叙述不正确的是
| A.金属腐蚀的本质是金属原子失去电子而被氧化 |
| B.将地下钢管与直流电源的正极相连,用来保护钢管 |
| C.电解饱和食盐水制氢氧化钠,可以用铁做阴极 |
| D.氢氧燃料电池中,氢气在负极发生氧化反应 |
将右图所示实验装置的K闭合,下列判断正确的是
| A.Zn电极上发生还原反应 |
| B.片刻后盐桥中的Cl-向乙装置中移动 |
| C.片刻后在a点滴加酚酞观察到滤纸变红色 |
| D.片刻后在b点滴加淀粉碘化钾溶液观察到滤纸无变化 |
早在1807年化学家戴维用电解熔融氢氧化钠制得钠: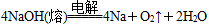 ;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠:
;后来盖·吕萨克用铁与熔融氢氧化钠作用也制得钠: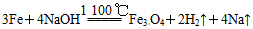 。下列有关说法正确的是
。下列有关说法正确的是
| A.电解熔融氢氧化钠制钠,阳极发生电解反应为2OH--2e-=H2↑+O2↑ |
| B.盖·吕萨克法制钠原理是利用铁的还原性比钠强 |
| C.若戴维法与盖·吕萨克法制得等量的钠,则两反应中转移的电子总数不同 |
| D.目前工业上常用电解熔融氯化钠法制钠(如上图),电解槽中石墨极为阴极,铁为阳极 |