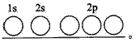题目内容
A.不锈钢是由铁、铬、镍、碳及众多不同元素所组成的合金,铁是主要成分元素,铬是第一主要的合金元素.其中铬的含量不能低于11%,不然就不能生成致密氧化膜CrO3防止腐蚀.
(1)基态碳(C)原子的轨道表示式为
 .
.
(2)[Cr(H2O)4Cl2]Cl?2H2O中Cr的配位数为
 .
.
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是
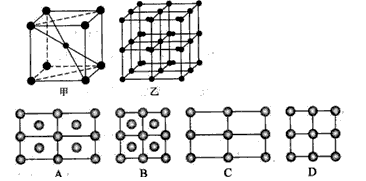
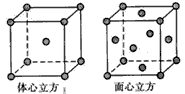
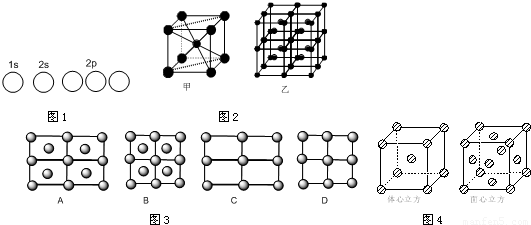
(4)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到A~B图中正确的是
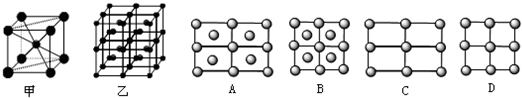
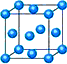
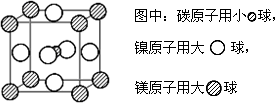
(5)据报道,只含镁、镍和碳三种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式


(1)基态碳(C)原子的轨道表示式为


(2)[Cr(H2O)4Cl2]Cl?2H2O中Cr的配位数为
6
6
;已知CrO5中Cr为+6价,则CrO5的结构式为

(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,呈四面体构型.423K时,Ni(CO)4分解为Ni和CO,从而制得高纯度的Ni粉.试推测:四羰基镍的晶体类型是
分子晶体
分子晶体
,与Ni(CO)4中配体互为等电子的离子是CN-、C22-
CN-、C22-
.(4)Fe的一种晶体如甲、乙所示,若按甲虚线方向切乙得到A~B图中正确的是
A
A
.
(5)据报道,只含镁、镍和碳三种元素的晶体竟然具有超导性.鉴于这三种元素都是常见元素,从而引起广泛关注.该晶体的结构可看作由镁原子和镍原子在一起进行面心立方密堆积,试写出该晶体的化学式
MgCNi3
MgCNi3
.晶体中每个镁原子周围距离最近的镍原子有12
12
个.

分析:(1)基态碳原子含有6个电子,2个电子排在1S轨道上,2个电子排在2s轨道上,2个电子排在2p轨道上,分占2个轨道,且方向相同;
(2)根据化学式确定其配位数;根据化学式判断配位数,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键注重Cr为+2价,以此书写结构式;
(3)沸点较低的晶体一般为分子晶体;Ni(CO)4中配体是CO,CO的等电子体是与其原子个数相等且价电子数相等的分子或离子;
(4)根据晶胞堆积形成较大晶体,按甲虚线方向切乙形成的纵截面分析;
(5)利用均摊法计算确定其化学式,利用沿X、Y、Z三轴切割的方法确定镍原子个数.
(2)根据化学式确定其配位数;根据化学式判断配位数,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键注重Cr为+2价,以此书写结构式;
(3)沸点较低的晶体一般为分子晶体;Ni(CO)4中配体是CO,CO的等电子体是与其原子个数相等且价电子数相等的分子或离子;
(4)根据晶胞堆积形成较大晶体,按甲虚线方向切乙形成的纵截面分析;
(5)利用均摊法计算确定其化学式,利用沿X、Y、Z三轴切割的方法确定镍原子个数.
解答:解:(1)碳原子核外有6个电子,根据电子排布规律知,其轨道表示式为 ,故答案为:
,故答案为: ;
;
(2)[Cr(H2O)4Cl2]Cl?2H2O中Cr与4个H2O,2个Cl-形成配位键,所以配位数为6,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键中Cr为+2价,则结构式为 ,
,
故答案为:6; ;
;
(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,应为分子晶体,与Ni(CO)4中配体互为等电子的离子是CN-、C22-;
故答案为:分子晶体;CN-、C22-;
(4)甲中Fe位于顶点和体心,乙由8个甲组成,按甲虚线方向切乙形成的纵截面边长不相等,则排除B、D,由于每个小晶胞中的体心含有1个Fe原子,则应为A,故答案为:A;
(5)该晶胞中,碳原子个数是1,镁原子个数=8×
=1,镍原子个数=6×
=3,所以其化学式为:MgCNi3,利用沿X、Y、Z三轴切割的方法知,晶体中每个镁原子周围距离最近的镍原子有4×3=12,
故答案为:MgCNi3;12.
 ,故答案为:
,故答案为: ;
;(2)[Cr(H2O)4Cl2]Cl?2H2O中Cr与4个H2O,2个Cl-形成配位键,所以配位数为6,CrO5中存在过氧键、Cr-O键、Cr=O,在4个Cr-O键中Cr为+1价,在Cr=O键中Cr为+2价,则结构式为
 ,
,故答案为:6;
 ;
;(3)金属镍粉在CO气流中轻微加热,生成无色挥发性液态Ni(CO)4,应为分子晶体,与Ni(CO)4中配体互为等电子的离子是CN-、C22-;
故答案为:分子晶体;CN-、C22-;
(4)甲中Fe位于顶点和体心,乙由8个甲组成,按甲虚线方向切乙形成的纵截面边长不相等,则排除B、D,由于每个小晶胞中的体心含有1个Fe原子,则应为A,故答案为:A;
(5)该晶胞中,碳原子个数是1,镁原子个数=8×
| 1 |
| 8 |
| 1 |
| 2 |
故答案为:MgCNi3;12.
点评:本题考查较为综合,题目难度较大,涉及化学式的确定、轨道式的书写、等电子体等知识点,化学式的确定、配位数的确定是常考知识点.

练习册系列答案
相关题目