题目内容
【题目】下列说法正确的有()个
①将铁屑放入稀HNO3中,证明Fe比H2活泼
②FeCl3腐蚀Cu 制印刷电路板是由于铁比铜的金属性强
③检验溶液中是否含有Fe2+,取少量待检验溶液,向其中加入少量新制氯水,再滴加KSCN 溶液,观察实验现象
④磁性氧化铁溶于稀硝酸的离子方程式为:3Fe2++4H++NO3-==3Fe3++NO↑+3H2O
⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中,制备Fe(OH)3胶体
⑥氢氧化铁与HI溶液反应的离子方程式为: Fe(OH)3+3H+==Fe3++3H2O
⑦铁与水蒸气在高温下的反应产物为Fe2O3 和H2
⑧1mol FeI2与足量氯气反应时转移的电子数为3NA
⑨检验Fe (NO3)2晶体是否氧化变质的方法是将Fe (NO3) 2样品溶于稀H2SO4后,滴加KSCN 溶液,观察溶液是否变红
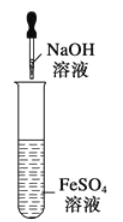
⑩图示装置能较长时间观察到Fe (OH) 2白色沉淀
A. 1 B. 2 C. 3 D. 4
【答案】A
【解析】①将铁屑放入稀HNO3中,硝酸具有强氧化性,生成氮的氧化物而不产生氢气,所以不能证明Fe比H2活泼,故①错误;②FeCl3具有强氧化性,可与Cu发生反应:2Fe3++Cu=2Fe2++Cu2+,与铁、铜的活泼性无关,故②错误; ③加入少量新制氯水,可将亚铁离子氧化成铁离子,所以试剂加入顺序不合理,应先加KSCN溶液无现象、再加氯水,故③错误;④磁性氧化铁为固体,应写成化学式,正确的离子方程式为3Fe3O4+NO3+28H+═9Fe3++14H2O+NO↑,故④错误;⑤将NaOH浓溶液滴加到饱和的FeCl3溶液中反应生成Fe(OH)3沉淀,应向沸水中滴加饱和氯化铁溶液来制备胶体,故⑤错误;⑥氢氧化铁与HI溶液反应生成的Fe3+与I-会发生氧化还原反应,正确的离子方程式为:2Fe(OH)3+6H++2I-=2Fe2++I2+6H2O,故⑥错误;⑦铁与水蒸气在高温下反应的产物是Fe3O4和H2,故⑦错误;⑧ FeI2与足量氯气发生反应的化学方程式为:2FeI2+3Cl2=2FeCl3+2I2,根据方程式可知,1molFeI2消耗1.5molCl2,转移电子3mol,转移的电子数为3NA,故⑧正确;⑨将Fe(NO3)2样品溶于稀H2SO4后,在酸性条件下,NO3-能把Fe2+氧化为Fe3+,滴加KSCN溶液变红,不能说明Fe(NO3)2晶体已经变质,故⑨错误;⑩要较长时间观察到Fe (OH) 2白色沉淀,必须在制取过程中尽可能减少和空气接触,而该装置中生成的Fe(OH)2与空气接触发生反应:4Fe(OH)2+O2+2H2O=4Fe(OH)3,故⑩错误;根据上述分析可知,只有⑧正确,故答案选A。

 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案