题目内容
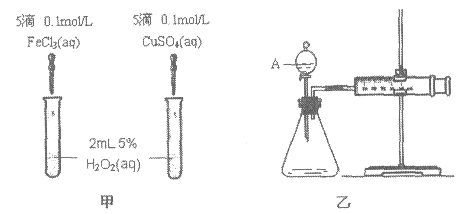
【题目】如图所示,在容器A中装有20℃的水50mL,容器B中装有1mol/L的盐酸50mL,试管C、D相连通,且其中装有红棕色NO2和无色N2O4的混合气体,并处于下列平衡:2NO2 N2O4 △H=-57kJ/mol,当向A中加入50gNH4NO3晶体使之溶解;向B中加入2g苛性钠时:

(1)C中的气体颜色______;(填“变浅” 或“变深”).
(2)若25℃时,起始时仅有NO2气体,达到平衡时,c(NO2)=0.0125mol/L,c(N2O4)=0.0321mol/L,则NO2的起始浓度为 _____________,NO2的转化率为________.
【答案】变浅 0.0767mol/L 83.7%
【解析】
(1)硝酸铵的溶解过程是吸热过程,温度降低,C中平衡正向移动;氢氧化钠溶解是放热过程、与盐酸反应放出热量,D中平衡逆向移动;
(2)根据四氧化二氮的平衡浓度,计算二氧化氮浓度变化量,进而人家是二氧化氮起始浓度与转化率。
(1)A中硝酸铵的溶解过程是吸热过程,溶解后C中温度降低,化学平衡2NO2N2O4,△H=-57kJ/mol,平衡会向着正反应方向移动,二氧化氮浓度减小,所以颜色变浅;
因此,本题正确答案是:变浅;
(2)设二氧化氮的初始浓度为cmol/L,根据题意信息可以知道:
2NO2 N2O4
初始浓度(mol/L):c 0
变化浓度(mol/L):c-0.0125 0.0321
平衡浓度(mol/L):0.0125 0.0321
则c-0.0125=2×0.0321,计算得出c=0.0767mol/L,
NO2的转化率为:![]() ×100%≈83.7%.
×100%≈83.7%.
因此,本题正确答案是:0.0767mol/L;83.7%。

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目