题目内容
(三选一)【化学与技术】
随着能源问题的进一步突出,利用热化学循环制氢的研究越发受到发达国家的青睐。最近的研究发现复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢,MnFe2O4的制备流程如下
随着能源问题的进一步突出,利用热化学循环制氢的研究越发受到发达国家的青睐。最近的研究发现复合氧化物铁酸锰(MnFe2O4)可用于热化学循环分解水制氢,MnFe2O4的制备流程如下
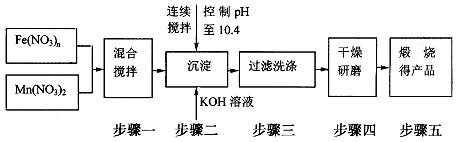
(1)原料Fe(NO3)n中n=____,投入原料Fe(NO3)n和Mn(NO3)2的物质的量之比应为________。
(2)步骤二中“连续搅拌”的目的是______,步骤三中洗涤干净的标准是_____________。
(3)利用MnFe2O4热化学循环制氢的反应可表示为:MnFeO4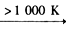 MnFe2O4-x+O2↑、MnFe2O4-x+xH2O →MnFe2O4+xH2↑,请认真分析上述两个反应并回答下列问题:
MnFe2O4-x+O2↑、MnFe2O4-x+xH2O →MnFe2O4+xH2↑,请认真分析上述两个反应并回答下列问题:
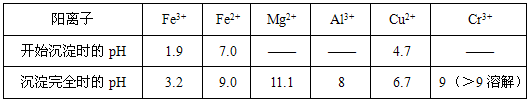
①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为________。
②该热化学循环制氢法的优点有(答两点即可)________________。
③该热化学循环制氢法尚有不足之处,进一步改进的方向是_______________。
(2)步骤二中“连续搅拌”的目的是______,步骤三中洗涤干净的标准是_____________。
(3)利用MnFe2O4热化学循环制氢的反应可表示为:MnFeO4
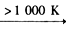 MnFe2O4-x+O2↑、MnFe2O4-x+xH2O →MnFe2O4+xH2↑,请认真分析上述两个反应并回答下列问题:
MnFe2O4-x+O2↑、MnFe2O4-x+xH2O →MnFe2O4+xH2↑,请认真分析上述两个反应并回答下列问题: ①若MnFe2O4-x中x=0.8,则MnFe2O4-x中Fe2+占全部铁元素的百分率为________。
②该热化学循环制氢法的优点有(答两点即可)________________。
③该热化学循环制氢法尚有不足之处,进一步改进的方向是_______________。
(1)3;2:1
(2)充分反应、沉淀完全;洗涤至流出液呈中性
(3)①80%;②过程简单、节约能量、无污染、物料廉价并可循环使用及氧气和氢气在不同步骤生成,不存在高温气体分离;③寻找合适的催化剂,使MnFe2O4的分解温度降低或找分解温度更低的氧化物(其他合理答案均可)
(2)充分反应、沉淀完全;洗涤至流出液呈中性
(3)①80%;②过程简单、节约能量、无污染、物料廉价并可循环使用及氧气和氢气在不同步骤生成,不存在高温气体分离;③寻找合适的催化剂,使MnFe2O4的分解温度降低或找分解温度更低的氧化物(其他合理答案均可)

练习册系列答案
相关题目
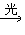 CH3CH2Cl+HCl
CH3CH2Cl+HCl 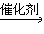 CH3CH2Cl
CH3CH2Cl