题目内容
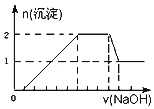
【题目】某无色溶液中可能含有H+、Na+、NH4+、Mg2+、Fe3+、Al3+、SO42﹣等离子中的几种,当向该溶液中加入某浓度的NaOH溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示.下列说法 一定正确的是( )
A. 一定存在H+、Mg2+、Al3+、NH4+,一定不存在Na+、SO42﹣、Fe3+
B. 一定存在H+、Al3+、NH4+、SO42﹣,可能存在Na+、Mg2+
C. 溶液中c(H+):c(Al3+):c(Mg2+)为1:1:2
D. 溶液中c(H+)/c(SO42﹣)比值小于等于2/9
【答案】D
【解析】该无色溶液中不含有棕黄色离子Fe3+。由图可知依次发生反应:H++OH-![]() H2O,Al3++3OH-
H2O,Al3++3OH-![]() Al(OH)3↓、Mg2++2
Al(OH)3↓、Mg2++2![]() -
-![]() Mg(OH)2↓,
Mg(OH)2↓,![]() +OH-
+OH-![]() NH3·H2O,Al(OH)3+OH-
NH3·H2O,Al(OH)3+OH-![]()
![]() +2H2O,可见含有H+、NH4+、Mg2+、Al3+,为了保持电荷守恒还要含有阴离子SO42﹣。A. 一定存在SO42﹣,故A错误;B. 没有溶于氢氧化钠溶液的沉淀是氢氧化镁,说明一定存在Mg2+,故B错误;C. 由图判断溶液中c(H+):c(Al3+):c(Mg2+)为1:1:1,故C错误;D. H+、NH4+、Mg2+、Al3+所带正电荷是H+的9倍,无法确定是否存在Na+,所以为了保持电荷守恒,溶液中c(H+)/c(SO42﹣)比值小于等于2/9,故D正确。故选D。
+2H2O,可见含有H+、NH4+、Mg2+、Al3+,为了保持电荷守恒还要含有阴离子SO42﹣。A. 一定存在SO42﹣,故A错误;B. 没有溶于氢氧化钠溶液的沉淀是氢氧化镁,说明一定存在Mg2+,故B错误;C. 由图判断溶液中c(H+):c(Al3+):c(Mg2+)为1:1:1,故C错误;D. H+、NH4+、Mg2+、Al3+所带正电荷是H+的9倍,无法确定是否存在Na+,所以为了保持电荷守恒,溶液中c(H+)/c(SO42﹣)比值小于等于2/9,故D正确。故选D。

练习册系列答案
相关题目