题目内容
【题目】(I)有下列各组微粒:(用①-⑤序号填空)
①12C和14C ②O2和O3 ③D2、T2 ④乙醇和二甲醚 ⑤冰和水
(1)互为同位素的是_________;
(2)互为同素异形体的是_________;
(3)互为同分异构体的是_________。
(II)写出下列微粒的电子式:
(4)NH4Cl______________。
(5)CaO2_____________。
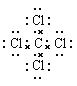
(6)CCl4____________。
(III)写出下列微粒的结构式:
(7)N2______________。
(8)H2O_____________。
【答案】 ① ② ④ 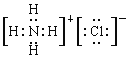
![]()
 N≡N H-O-H
N≡N H-O-H
【解析】
(I)(1)质子数相同中子数不同的同一种元素的不同核素互为同位素,则互为同位素的是12C和14C,答案选①;
(2)由同一种元素形成的不同单质互为同素异形体,则互为同素异形体的是O2和O3,答案选②;
(3)分子式相同结构不同的化合物互为同分异构体,则互为同分异构体的是乙醇和二甲醚,答案选④。
(II)(4)NH4Cl是离子化合物,电子式为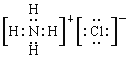 。
。
(5)CaO2中含有离子键,电子式为![]() 。
。
(6)CCl4是共价化合物,含有共价键,电子式为 。
。
(III)用短线“—”表示原子之间所形成的一对共用电子进而表示物质结构的式子称为结构式,则
(7)N2分子中含有三键,结构式为N≡N。
(8)H2O的结构式为H-O-H。

【题目】一定温度下,向10 mL 0.40 mol·L-1 H2O2溶液中加入适量FeCl3溶液,不同时刻测得生成O2的体积(已折算为标准状况)如下表所示:
t / min | 0 | 2 | 4 | 6 |
V(O2) / mL | 0 | 9.9 | 17.2 | 22.4 |
资料显示,反应分两步进行:① 2Fe3++H2O2 == 2Fe2++O2↑+2H+,② H2O2+2Fe2++2H+ == 2H2O+2Fe3+。反应过程中能量变化如下图所示。下列说法错误的是
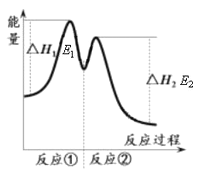
A. Fe3+的作用是增大过氧化氢的分解速率
B. 反应①是吸热反应、反应②是放热反应
C. 反应2H2O2(aq) == 2H2O(l)+O2(g)的ΔH=E1-E2<0
D. 0~6 min的平均反应速率:v(H2O2)=3.33×10-2 mol·L-1·min-1