题目内容
15.下列实验操作、现象和结论均正确的是( )| 选项 | 操作 | 现象 | 结论 |
| A | 向FeSO4溶液中滴入少量酸性KMnO4溶液 | KMnO4溶液紫色褪去 | Fe2+有氧化性 |
| B | 向Na2SiO3溶液中通入适量的CO2 | 产生白色胶状物质 | 酸性:H2CO3>H2SiO3 |
| C | 将新制氯水和NaBr溶液在试管中混合后,加入CCl4,振荡,静置 | 下层溶液呈橙红色 | 氧化性:Cl2>Br2 |
| D | 向Al2(SO4)3溶液中滴加过量氨水 | 溶液先浑浊后澄清 | Al3+与NH3•H2O不能大量共存 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.发生氧化还原反应,Fe元素的化合价升高,Mn元素的化合价降低;
B.发生强酸制取弱酸的反应;
C.氯水置换出溴,加四氯化碳萃取后有机层在下层;
D.反应生成氢氧化铝和硫酸铵.
解答 解:A.向FeSO4溶液中滴入少量酸性KMnO4溶液,由现象可知发生氧化还原反应,Fe元素的化合价升高,Fe2+有还原性,故A错误;
B.向Na2SiO3溶液中通入适量的CO2,由现象可知发生强酸制取弱酸的反应,则酸性为H2CO3>H2SiO3,故B正确;
C.由操作和现象可知氯水置换出溴,加四氯化碳萃取后有机层在下层,下层溶液呈橙红色,则氧化性:Cl2>Br2,故C正确;
D.反应生成氢氧化铝和硫酸铵,则溶液变浑浊,氢氧化铝不能溶解在氨水中,故D错误;
故选BC.
点评 本题考查化学实验方案的评价,为高频考点,涉及氧化还原反应、酸性比较、萃取及氢氧化铝的两性等,把握物质的性质、反应原理为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
 同步奥数系列答案
同步奥数系列答案
相关题目
5.聚乳酸是一种生物降解塑料,结构简式为 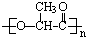 .下列说法正确的是( )
.下列说法正确的是( )
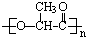 .下列说法正确的是( )
.下列说法正确的是( )| A. | 聚乳酸的相对分子质量是72 | B. | 聚乳酸的分子式是C3H4O2 | ||
| C. | 乳酸的分子式是C3H6O2 | D. | 聚乳酸可以通过水解降解 |
6.有机物M的结构简式如图所示,下列说法正确的是( )
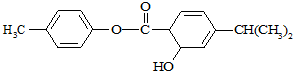

| A. | 分子式为C17H18O3 | |
| B. | M中有4个饱和碳原子 | |
| C. | M可以使溴水和酸性高锰酸钾溶液褪色,但它们的反应类型不同 | |
| D. | 1mol M常温下最多可以与6 mol H2反应 |
3.向4.0L容器中充入0.70 mol SO2和0.40 mol O2,4s后测得剩余SO2 0.30 mol,则v(O2)为( )
| A. | 0.10 mol•L-1•s-1 | B. | 0.025 mol•L-1•s-1 | ||
| C. | 0.50 mol•L-1•s-1 | D. | 0.0125 mol•L-1•s-1 |
10.下列有关实验操作、现象和解释或结论都正确的是( )
| 实验操作 | 现象 | 解释或结论 |
| 在稀硝酸中加入过量的铁粉,充分反应后滴入KSCN溶液 | 溶液呈红色 | HNO3将Fe氧化为Fe3+ |
| AgI沉淀中滴入KCl溶液 | 有白色沉淀出现 | AgCl比AgI更难溶 |
| Cl2通入品红溶液中 | 溶液褪色 | Cl2具有漂白性 |
| 用玻璃棒蘸取浓氨水点到红色石蕊试纸上 | 试纸变蓝色 | 浓氨水呈碱性 |
| A. | A | B. | B | C. | C | D. | D |
20.两种醇的混合物4.176g与足量金属钠反应得到氢气1.344L(标况状况),该混合物中,两种醇的物质量之比为( )
| A. | 乙二醇和丙三醇是1:1 | B. | 乙醇和乙二醇是1:2 | ||
| C. | 甲醇和乙醇是5:1 | D. | 甲醇和乙醇是4:1 |
7.下列分离方法中,和物质的溶解度无关的是( )
| A. | 萃取 | B. | 纸上层析 | C. | 过滤 | D. | 蒸馏 |
8. 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,且最外层只有一个电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,且最外层只有一个电子.
(1)Y原子核外共有7种不同运动状态的电子,T原子的价层电子排列式3d104s1.
(2)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp.
(3)Z 与R能形成化合物甲,1mol甲中含4mol共价键,甲与氢氟酸反应,生成物的分子空间构型分别为正四面体形、V形
(4)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低,Mg2+的半径比Na+的半径小,电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高
(5)向T的硫酸盐溶液中逐滴加入Y的氢化物的水溶液至过量,反应的离子方程式为Cu2++2 NH3•H2O=Cu(OH)2↓+2NH4+、Cu(OH)2+4NH3=[Cu(NH3)4]2++2OH-
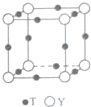
(6)T与Y形成的晶体的晶胞结构如图所示,Y离子的配位数是6..设晶胞棱长为acm,密度为 bg•cm-3,则阿伏伽德罗常数可表示为$\frac{206}{b{a}^{3}}$(用含a、b的式子表示)
 原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,且最外层只有一个电子.
原子序数依次增大的X、Y、Z、G、Q、R、T七种元素,核电荷数均小于36.已知X的一种1:2型氢化物分子中既有σ键又有π键,且所有原子共平面;Z的L层上有2个未成对电子;Q原子s能级与p能级电子数相等;G为金属元素;R单质是制造各种计算机、微电子产品的核心材料;T处于周期表的ds区,且最外层只有一个电子.(1)Y原子核外共有7种不同运动状态的电子,T原子的价层电子排列式3d104s1.
(2)由X、Y、Z形成的离子ZXY-与XZ2互为等电子体,则ZXY-中X原子的杂化轨道类型为sp.
(3)Z 与R能形成化合物甲,1mol甲中含4mol共价键,甲与氢氟酸反应,生成物的分子空间构型分别为正四面体形、V形
(4)G、Q、R氟化物的熔点如下表,造成熔点差异的原因为NaF与MgF2为离子晶体,SiF4为分子晶体,故SiF4的熔点低,Mg2+的半径比Na+的半径小,电荷数高,晶格能MgF2>NaF,故MgF2的熔点比NaF高
| 氟化物 | G的氟化物 | Q的氟化物 | R的氟化物 |
| 熔点/K | 993 | 1539 | 183 |
(6)T与Y形成的晶体的晶胞结构如图所示,Y离子的配位数是6..设晶胞棱长为acm,密度为 bg•cm-3,则阿伏伽德罗常数可表示为$\frac{206}{b{a}^{3}}$(用含a、b的式子表示)
9.用如图所示的实验装置完成对应的实验(部分仪器已省略),不能达到实验目的是( )
| A. |  制取纯净氢氧化亚铁 | B. | 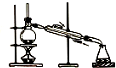 石油的蒸馏 | ||
| C. | 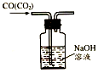 除去CO气体中的CO2气体 | D. | 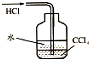 吸收HCl |