题目内容
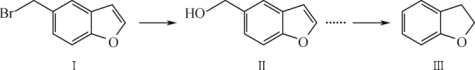
【题目】高聚物G、I可用于生产全生物降解塑料,在“白色污染”日益严重的今天有着重要的作用。有关转化关系如下:

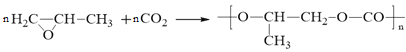
已知:①![]()
②H的分子中有一个“—O—”结构的三元环
③含有结构的有机物分子不能稳定存在,易失水形成![]() →
→![]()
请回答下列问题:
(1)写出H的结构简式___________
(2)写出H转化为I的化学方程式___________
(3)某化合物M分子式为C4H8O3,写出符合下列条件M的同分异构体的结构简式____________
①与化合物F具有相同的官能团 ②官能团不连在同一个碳上
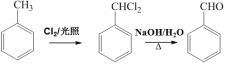
(4)依据上述合成路线,设计以甲苯![]() 为原料制备
为原料制备![]() 的合成路线(无机原料任意选择,合成路线用流程图表示)_______________合成路线流程图示例:
的合成路线(无机原料任意选择,合成路线用流程图表示)_______________合成路线流程图示例:
![]() 。
。
【答案】![]()
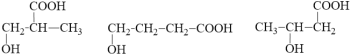
【解析】
B的结构简式为CH2=CHCH3,C为CH2BrCHBrCH3,D为CH2OHCHOHCH3,E为CH3COCOOH,F为CH3CHOHCOOH,H的分子中有一个“—O—”结构的三元环,说明H 的结构为![]() 。
。
(1)化合物H为结构简式为 ![]() 。(2)I为全生物降解塑料,即I应含有酯基官能团,所以有H和二氧化碳反应生成I 的方程式为:
。(2)I为全生物降解塑料,即I应含有酯基官能团,所以有H和二氧化碳反应生成I 的方程式为: 。(3) 某化合物M分子式为C4H8O3,与F具有相同的官能团,则有羟基和羧基,官能团不连在同一个碳原子上,所以,可能的结构为
。(3) 某化合物M分子式为C4H8O3,与F具有相同的官能团,则有羟基和羧基,官能团不连在同一个碳原子上,所以,可能的结构为 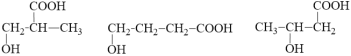 。 (4).以甲苯为原料制备苯甲醛,即先将甲基发生卤代反应,再将卤代烃发生水解反应,根据一个碳原子连接两个羟基,会自动变为醛基进行分析,合成路线为
。 (4).以甲苯为原料制备苯甲醛,即先将甲基发生卤代反应,再将卤代烃发生水解反应,根据一个碳原子连接两个羟基,会自动变为醛基进行分析,合成路线为 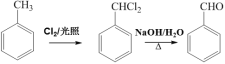 。
。

【题目】下面a~e是中学化学实验中常见的几种定量仪器:a.量筒 b.容量瓶 c.滴定管 d.托盘天平 e.温度计
(1)无“0”刻度的是________(填字母)。
(2)下列操作合理的是________(填字母)。
A.用25 mL碱式滴定管量取20.00 mL NaHCO3溶液
B.用托盘天平准确称量10.20 g碳酸钠固体
C.用100 mL量筒量取3.2 mL浓硫酸
D.用500 mL容量瓶配制1 mol·L-1的氢氧化钠溶液495.5 mL
(3)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为________mL。
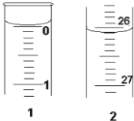
(4)某学生根据三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理数据列出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=________ mol·L-1。
(5)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.碱式滴定管用蒸馏水洗净后立即取用25.00 mL待测碱溶液注入锥形瓶进行滴定
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中然后用来滴定