题目内容
【题目】下面a~e是中学化学实验中常见的几种定量仪器:a.量筒 b.容量瓶 c.滴定管 d.托盘天平 e.温度计
(1)无“0”刻度的是________(填字母)。
(2)下列操作合理的是________(填字母)。
A.用25 mL碱式滴定管量取20.00 mL NaHCO3溶液
B.用托盘天平准确称量10.20 g碳酸钠固体
C.用100 mL量筒量取3.2 mL浓硫酸
D.用500 mL容量瓶配制1 mol·L-1的氢氧化钠溶液495.5 mL
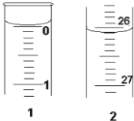
(3)某学生欲用已知物质的量浓度的盐酸来测定未知物质的量浓度的氢氧化钠溶液,若滴定开始和结束时,酸式滴定管中的液面如图所示:则所用盐酸的体积为________mL。
(4)某学生根据三次实验分别记录有关数据如下表:
滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.100 0 mol·L-1盐酸的体积/mL | ||
滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
请选用其中合理数据列出该氢氧化钠溶液物质的量浓度(计算结果保留4位有效数字):c(NaOH)=________ mol·L-1。
(5)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是________(填字母)。
A.中和滴定达终点时俯视滴定管内液面读数
B.碱式滴定管用蒸馏水洗净后立即取用25.00 mL待测碱溶液注入锥形瓶进行滴定
C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中然后用来滴定
【答案】ab AD 26.10 0.104 4 CD
【解析】
(1)量筒小刻度在下,故不需要0刻度;容量瓶只有一个量程刻度;滴定管、托盘天平、温度计均有0刻度;因此,本题正确答案是:ab。
(2)A. 碱式滴定管可以读数读到0.01 mL,合理;
B.托盘天平只能读到0.1g,不能称量10.20 g碳酸钠固体,不合理;
C. 用100 mL量筒量取3.2 mL浓硫酸,产生较大误差,应选用10 mL量筒,不合理;
D. 实验室没有495.5 mL 容量瓶,故选用500 mL容量瓶,合理;
综上所述,本题选AD 。
(3)滴定管的0刻度在上方,故图1、2正确;0-1刻度间每一小格为0.10mL,滴定开始时如图1显示0.00mL,结束时图2显示26.10mL,可以知道则所用盐酸溶液的体积为26.10-0.00=26.10 mL;因此,本题正确答案是:26.10。
(4)根据数据的有效性,舍去第2组数据,则1、3组平均消耗V(盐酸)=(26.11+26.09)/2=26.10mL,根据反应方程式HCl+NaOH=NaCl+H2O;0.0261×0.1000=0.025×c(NaOH),则c(NaOH)=0.1044 mol·L-1;综上所述,本题答案是:0.1044。
(5)A.读取盐酸体积时,滴定结束时俯视读数,造成V(标准)偏小,根据c(待测)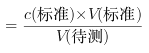 ,可以知道,测定c(NaOH)偏低,故A错误;
,可以知道,测定c(NaOH)偏低,故A错误;
B.碱式滴定管用蒸馏水洗净后立即取用25.00 mL待测碱溶液注入锥形瓶进行滴定,相当于稀释,造成c(NaOH)偏低,故B错误;
C.酸式滴定管未用标准盐酸溶液润洗就直接注入标准盐酸溶液,标准液的浓度偏小,造成V(标准)偏大,根据c(待测)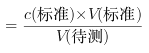 ,可以知道,测定c(NaOH)偏大,故C正确;
,可以知道,测定c(NaOH)偏大,故C正确;
D.把配好的标准溶液倒入刚用蒸馏水洗净的试剂瓶中标准液的浓度偏小,造成V(标准)偏大,根据c(待测)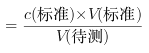 ,可以知道,测定 c(NaOH)偏大,故D正确;
,可以知道,测定 c(NaOH)偏大,故D正确;
综上所述,本题选CD。

【题目】[2016·新课标I]锗(Ge)是典型的半导体元素,在电子、材料等领域应用广泛。回答下列问题:
(1)基态Ge原子的核外电子排布式为[Ar]_______________,有__________个未成对电子。
(2)Ge与C是同族元素,C原子之间可以形成双键、叁键,但Ge原子之间难以形成双键或叁键。从原子结构角度分析,原因是______________________________。
(3)比较下列锗卤化物的熔点和沸点,分析其变化规律及原因______________________________。
GeCl4 | GeBr4 | GeI4 | |
熔点/℃ | 49.5 | 26 | 146 |
沸点/℃ | 83.1 | 186 | 约400 |
(4)光催化还原CO2制备CH4反应中,带状纳米Zn2GeO4是该反应的良好催化剂。Zn、Ge、O电负性由大至小的顺序是______________________________。
(5)Ge单晶具有金刚石型结构,其中Ge原子的杂化方式为_______________,微粒之间存在的作用力是_______________。
(6)晶胞有两个基本要素:
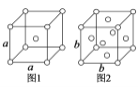
①原子坐标参数,表示晶胞内部各原子的相对位置。如图为Ge单晶的晶胞,其中原子坐标参数A为(0,0,0);B为(![]() ,0,
,0,![]() );C为(
);C为(![]() ,
,![]() ,0)。则D原子的坐标参数为_______________。
,0)。则D原子的坐标参数为_______________。
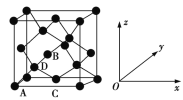
②晶胞参数,描述晶胞的大小和形状。已知Ge单晶的晶胞参数a=565.76 pm,其密度为_____g·cm3(列出计算式即可)。