题目内容
【题目】实验室从含溴化氢的废液中提取溴单质,下列装置能达到实验目的的是( )
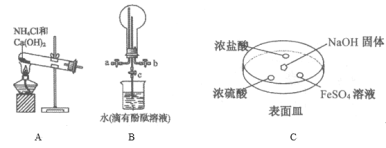
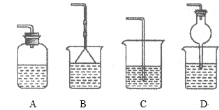
A. 氧化废液中的溴化氢
氧化废液中的溴化氢
B. 分离CCl4和水层
分离CCl4和水层
C. 分离四氯化碳和液溴
分离四氯化碳和液溴
D. 密封存放单质溴
密封存放单质溴
【答案】B
【解析】
A. 由于Cl2有强的氧化性,会把HBr中的溴元素氧化为Br2,为使物质充分发生反应,应该把导气管伸入到液面以下,故不能用装置甲氧化废液中的溴化氢,故A错误;
B. 由于水的密度比四氯化碳小,二者是互不相溶的两种液体物质,因此可以用分液的方法分离,故B正确;
C. 四氯化碳和液溴是沸点不同的互溶的两种液态物质,用蒸馏的方法分离时,一个把温度计的水银球放在蒸馏烧瓶的支管口附近,不能在液面一下,因此不能用装置丙分离四氯化碳和液溴,故C错误;
D. 溴容易挥发,在保存时常加些水形成水封,由于溴有强的氧化性,会与橡胶发生反应,所以应该使用玻璃塞密封保存在,并加水形成水封,故D错误;
答案选B。

 备战中考寒假系列答案
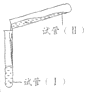
备战中考寒假系列答案【题目】某学习小组学习了亚铁盐的性质后,欲探究FeSO4溶液分别与Na2CO3溶液、NaHCO3溶液的反应。已知:Fe(OH)2和FeCO3均为白色沉淀,不存在Fe(HCO3)2。实验操作及现象记录如下:
实验 | 试剂 | 操作及现象 | ||
试管(I) | 试管(II) | |||
(试管容积为50 mL) | 实验a | 1.0 mol·L-1 FeSO4溶液 24 mL | 1.0 mol·L-1 Na2CO3溶液24mL | 倾倒完后,迅速用胶塞塞紧试管I的口部,反复上下颠倒摇匀,使反应物充分混合 反应过程中无气泡产生,生成白色絮状沉淀 放置1.5~2 h后,白色絮状沉淀转化为白色颗粒状沉淀 |
实验b | 1.0 mol·L-1 FeSO4溶液 10 mL | 1.0 mol·L-1 NaHCO3溶液 20 mL | 倾倒完后,迅速产生白色颗粒状沉淀和大量气泡。振荡,经2~4 min后液面上方试管内壁粘附的白色颗粒状沉淀物变成红褐色 | |
(1)甲同学认为实验a中白色颗粒状沉淀是FeCO3,写出该反应的离子方程式:________;他为了证实自己的观点,进行实验:取少量白色颗粒状沉淀,加入________,发现产生大量气泡。
(2)乙同学推测实验a的白色颗粒状沉淀中还可能含有Fe(OH)2,他将实验a中两种溶液体积均改成15 mL后再进行实验,证实了他的推测。能证明Fe(OH)2存在的实验现象是_________。
(3)实验b中白色颗粒状沉淀主要成分也为FeCO3,写出生成FeCO3的离子方程式:________。
(4)实验b中液面上方试管内壁粘附的白色颗粒状沉淀物变成红褐色,主要原因是潮湿的FeCO3被氧气氧化,写出该反应的化学方程式:__________。
(5)乙同学反思,实验a中含有Fe(OH)2,实验b中几乎不含有Fe(OH)2,对比分析出现差异的原因是_________。