题目内容
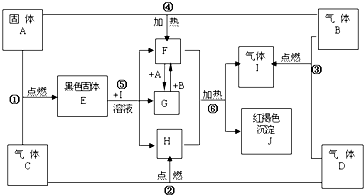
物质A、B、C、D、E、F、G、H、I、J、K有下图转化关系,其中气体D、E为单质,按要求回答下列问题.

(1)金属A元素在周期表的位置是
(2)写出反应“C→F”的离子方程式
(3)写出反应“I→J”的离子方程式
(4)写出F与NaOH溶液反应生成G的化学方程式

(1)金属A元素在周期表的位置是
第3周期第ⅢA族
第3周期第ⅢA族
,G的化学式是NaAlO2
NaAlO2
.(2)写出反应“C→F”的离子方程式
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
Al3++3NH3?H2O=Al(OH)3↓+3NH4+
;(3)写出反应“I→J”的离子方程式
2Fe2++Cl2=2Fe3++2Cl-
2Fe2++Cl2=2Fe3++2Cl-
;(4)写出F与NaOH溶液反应生成G的化学方程式
Al(OH)3+NaOH═NaAlO2+2H2O
Al(OH)3+NaOH═NaAlO2+2H2O
.分析:K为红褐色沉淀,则应为Fe(OH)3,则溶液J中含有Fe3+,气体E是黄绿色气体判断为Cl2,D应为H2,E应为氧化性气体Cl2,B应为HCl,则I为FeCl2,J为FeCl3,白色沉淀F能溶于过量NaOH溶液,则F为Al(OH)3,G为NaAlO2,A为Al,C为AlCl3,根据物质的性质判断所发生的反应,并解答该题.
解答:解:(1)K为红褐色沉淀,则应为Fe(OH)3,则溶液J中含有Fe3+,气体E是黄绿色气体判断为Cl2,D应为H2,E应为氧化性气体Cl2,B应为HCl,则I为FeCl2,J为FeCl3,白色沉淀F能溶于过量NaOH溶液,则F为Al(OH)3,G为NaAlO2,A为Al,C为AlCl3;则A为Al在周期表中位于第3周期第ⅢA族,
故答案为:第3周期第ⅢA族;NaAlO2 ;
(2)C→F是AlCl3氨水反应生成氢氧化铝和氯化铵,反应的离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(3)反应“I→J”是FeCl2和Cl2发生反应生成氯化亚铁,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)F与NaOH溶液反应生成G是Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠和水,反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O,
故答案为:Al(OH)3+NaOH═NaAlO2+2H2O.
故答案为:第3周期第ⅢA族;NaAlO2 ;
(2)C→F是AlCl3氨水反应生成氢氧化铝和氯化铵,反应的离子方程式为Al3++3NH3?H2O=Al(OH)3↓+3NH4+,
故答案为:Al3++3NH3?H2O=Al(OH)3↓+3NH4+;
(3)反应“I→J”是FeCl2和Cl2发生反应生成氯化亚铁,反应离子方程式为2Fe2++Cl2=2Fe3++2Cl-,
故答案为:2Fe2++Cl2=2Fe3++2Cl-;
(4)F与NaOH溶液反应生成G是Al(OH)3和氢氧化钠溶液反应生成偏铝酸钠和水,反应的化学方程式为Al(OH)3+NaOH═NaAlO2+2H2O,
故答案为:Al(OH)3+NaOH═NaAlO2+2H2O.
点评:本题考查了物质转化关系的分析,物质性质的应用判断,主要是铁及其化合物,铝及其化合物发生反应的现象和产物的判断,题目难度中等.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目