题目内容
【题目】下表列出了 AH八种元素在周期表中的位置。
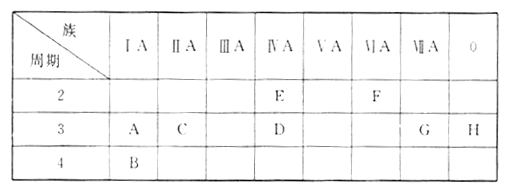
(1)这八种元素中化学性质最不活泼的是____________(填元素符号)。
(2)A、B、G 种元素对应的简单离子半径由大到小的顺序为______________(用离子符号表示)。
(3)F元素与氢元素能形成18电子的化合物,该化合物的化学式为_______________。 (4) C元素与G元素形成化合物的电子式是____________________。
(5)A、D两元素最高价氧化物对应的水化物之间发生反应的离子方程式为________________。
【答案】 Ar Cr->K+>Na+ H2O2 [![]() ]-Mg2+[
]-Mg2+[![]() ]- 2OH-+H2SiO3=SiO32-+2H2O (或其他合理答案)
]- 2OH-+H2SiO3=SiO32-+2H2O (或其他合理答案)
【解析】根据元素在周期表中的位置可知:A为Na元素,B为K元素,C为Mg元素,D为Si元素,E为C元素,F为O元素,G为Cl元素,H为Ar元素。
(1)这八种元素中化学性质最不活泼的是Ar元素,故答案为:Ar;
(2)钠离子只有2个电子层,离子半径最小,钾离子和氯离子的电子层结构相同,但钾的原子序数大于氯,则离子半径氯离子大于钾离子,3种元素对应的简单离子半径由大到小的顺序为Cr->K+>Na+,故答案为:Cr->K+>Na+;
(3) F为O元素,F元素与氢元素能形成18电子的化合物为双氧水,化学式为H2O2,故答案为:H2O2;
(4) C为Mg元素,G为Cl元素,氯化镁的电子式为![]() ,故答案为:
,故答案为:![]() ;
;
(5)氢氧化钠与硅酸反应生成硅酸钠和水,反应的离子方程式为2OH-+H2SiO3=SiO32-+2H2O,故答案为:2OH-+H2SiO3=SiO32-+2H2O。

【题目】下列实验操作或事实与预期实验目的或所得结论一致的是
选项 | 实验操作或事实 | 实验目的或结论 |
A | 淡黄色试液 | 说明原溶液中一定含有FeCl3 |
B | Br2 | 制备少量KBr溶液 |
C | 无色试液 | 说明原溶液中一定不含钾元素 |
D | H3PO3+2NaOH(足量)=Na2HPO3+2H2O | H3PO3属于三元酸 |
A. A B. B C. C D. D
【题目】下列选用的除杂试剂和实验操作都正确的(已知2Br﹣+Cl2═Br2+2Cl﹣)是( )
选项 | 物质 | 杂质 | 除杂试剂 | 操作方法 |
A | CaCl2溶液 | 稀盐酸 | 过量碳酸钙 | 过滤 |
B | NaCl溶液 | NaBr | 稍过量氯水、乙醇 | 萃取、分液 |
C | NaCl溶液 | Na2CO3 | 适量硝酸钙溶液 | 过滤 |
D | O2 | CO | 氧化铜 | 通过灼热的氧化铜 |
A.A
B.B
C.C
D.D