��Ŀ����
����Ŀ��1869�������ѧ���Ž��з��Ƴ���һ��Ԫ�����ڱ����������γɵ����ڱ��������ڶѧ�ҵļ���Ŭ��������142�꣬Ԫ�����ڱ�������Ԫ��λ���ԵĹ�ϵ����ʾ��Ԫ�ؼ��������ϵ����ͼ��Ԫ�����ڱ���һ���֣��ش��������⡣
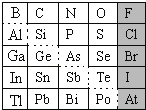
��1��Ԫ��Ga��Ԫ�����ڱ��е�λ��Ϊ��___��д�����ں��壩��
��2��Sn���������Ϊ___��Cl������������Ӧˮ����Ļ�ѧʽΪ___��As����̬�⻯��Ϊ___��
��3������Ԫ�������ɣ��ƶϣ�
����Ӱ����Ԫ���⻯�����ȶ�����ߵ���___���ѧʽ����
��H3AsO4��H2SeO4������ǿ����H3AsO4___H2SeO4�����������������=������
���⻯��Ļ�ԭ�ԣ�H2O___H2S�����������������=������
��4������ͼ�зֽ��ߣ����߲��֣�����Ѱ��___������ţ���
A.�����Ĵ��� B.�뵼����� C.�Ͻ���� D.ũҩ
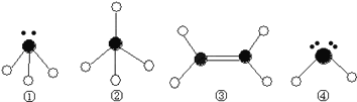
��5����Se2Cl2�����������Լ��������ʽΪ___��
������Se��������In����һ�ֿ�Ӧ����δ�������豸�����Ͱ뵼����ϡ�����˵����ȷ����___������ĸ����
A.ԭ�Ӱ뾶��In��Se
B.In�Ľ����Ա�Seǿ
C.In�Ľ����Ա�Al��
D.�������Ļ�ѧʽΪInSe2
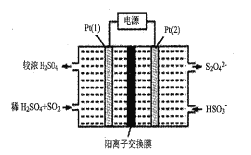
�۹�ҵ�ϳ��ӵ�ұͭ������������ȡ��������������������ͨ��������Cu2Se����Һ�е�HClO����ΪH2SeO3��CuCl2����Ӧ��HClO��Cu2Se�����ʵ���֮��Ϊ___��
��6�������ʵ��Ƚ�C��Si�ķǽ�����ǿ��˳�ɹ�ѡ���ҩƷ�У�CaCO3���塢ϡ���ᡢ���ᡢ����NaHCO3��Һ������Na2CO3��Һ����������Һ����ѧ����������Ҫѡ��
ʵ�鲽�� | ʵ����������� |
���Թ��м���___���ټ���___������������ͨ��___ϴ����ͨ��___�� | ����___�����ۣ��ǽ�����C��Si |
���𰸡�4����A +4 HClO4 AsH3 HF �� �� B 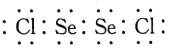 AB 4��1 CaCO3���� ���� NaHCO3��Һ Na2SiO3��Һ ���ɰ�ɫ��״����
AB 4��1 CaCO3���� ���� NaHCO3��Һ Na2SiO3��Һ ���ɰ�ɫ��״����
��������
��1��Ga��Alͬ���壬��Al����һ�����ڣ����������ڣ��ڢ�A�壬�ʴ�Ϊ��4����A��
��2��Sn��̼ͬ���壬�����+4�ۣ�Cl�������+7�ۣ�����������Ӧˮ����Ļ�ѧʽΪHClO4��As��NԪ��ͬ���壬�����������-3�ۣ�As����̬�⻯��ΪAsH3��
�ʴ�Ϊ��+4��HClO4��AsH3��
��3����ͬ����Ԫ�ش��ϵ��£��⻯���ȶ��Լ�����ͬ����Ԫ�ش��ҵ����⻯���ȶ��Լ�����������Ӱ����Ԫ���⻯�����ȶ�����ߵ���HF���ʴ�Ϊ��HF��
��As��Seͬһ���ڣ�ͬ����Ԫ�ش��ҵ�����ۺ���������Լ���������H3AsO4��H2SeO4������ǿ����H3AsO4��H2SeO4���ʴ�Ϊ������
���⻯��Ļ�ԭ�ԣ�H2O��H2S���ʴ�Ϊ������
��4�����ڽ����ͷǽ����ķֽ��߸�����Ѱ�Ұ뵼����ϣ��ʴ�Ϊ��B��
��5��������ԭ������Ϊ34�������ͬ����Ԫ�أ�λ��S���·�����λ�����ڱ��������ڢ�A�壬Se2Cl2�ĵ���ʽΪ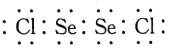 ���ʴ�Ϊ��
���ʴ�Ϊ��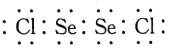 ��
��
������In������ͬ���ұ������������Ӳ㣬λ�ڵ�������IIIA�壬
A�����Ӳ�Խ�࣬ԭ�Ӱ뾶Խ����ԭ�Ӱ뾶��In��Se����A��ȷ��
B��Ԫ�����ڱ������·�Ԫ�صĽ�����ǿ����In�Ľ����Ա�Seǿ����B��ȷ��
C��ͬ������ϵ��½�������ǿ����In�Ľ����Ա�Alǿ����C����
D���������Ļ�ѧʽΪIn2Se3����D����
�ʴ�Ϊ��AB��
��Cu2Se����Һ�е�HClO����ΪH2SeO3��CuCl2����֪ClԪ�صĻ��ϼ���+1�۽���Ϊ-1�ۣ�CuԪ�صĻ��ϼ���+1������Ϊ+2�ۡ�SeԪ�صĻ��ϼ���-2������Ϊ+4�ۣ��ɵ����غ��֪HClO��Cu2Se�����ʵ���֮��Ϊ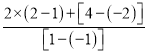 =4��1���ʴ�Ϊ��4��1��
=4��1���ʴ�Ϊ��4��1��
��6��C��Si�ķǽ�����ǿ��˳��ΪC��Si�����Ը���̼������ǿ�ڹ�����֤������ѧ��Ӧ�У�ǿ������Ƶ����ᣬ�����Թ��м���CaCO3���壬�ټ������ᣬ����������ͨ��NaHCO3��Һϴ����ͨ��Na2SiO3��Һ�����ɰ�ɫ��״��������̼������ǿ�ڹ��ᣬ���ۣ��ǽ�����C��Si��
�ʴ�Ϊ��CaCO3���壻���ᣬNaHCO3��Һ��Na2SiO3��Һ���������ɰ�ɫ��״������

 �ܿ�����ĩ��̾�ϵ�д�
�ܿ�����ĩ��̾�ϵ�д�