题目内容
【题目】三氯氧磷(POCl3)广泛用于农药、医药及阻燃剂的生产工业等,工业制备三氯氧磷的过程中会产生副产品亚磷酸(H3PO3)。
(1)三氯氧磷可通过氯化水解法制备,由三氯化磷、水、氯气加热反应生成,则该反应中另一产物的化学式为____________。
(2)已知H3PO3为二元弱酸。某温度下,0.1 mol·L-1的H3PO3溶液中c(H+) = 2.5×10-2 mol·L-1。则该温度下H3PO3的第一步电离的平衡常数Ka1=_______(H3PO3的第二步电离忽略不计,保留两位有效数字)。
(3)亚磷酸具有强还原性,可将Cu2+还原为金属单质,亚磷酸与硫酸铜溶液反应的化学方程式为_____________________。
(4)工业上生产三氯氧磷的同时会产生含磷废水(主要成分为H3PO4、H3PO3)。向废水中先加入适量漂白粉,再加入生石灰调节pH将磷元素转化为磷酸的钙盐沉淀并回收。若处理后的废水中 c(PO43-)=4×10-7 mol·L-1,则溶液中c(Ca2+)=___________mol·L-1。{已知Ksp=[Ca3(PO4)2]=2×10-29 }
【答案】 HCl 8.3×10-3 H3PO3+CuSO4+H2O=Cu↓+H3PO4+H2SO4 5×l0-6
【解析】(1)三氯氧磷(POCl3)由三氯化磷、水、氯气加热反应生成,根据质量守恒以及氧化还原反应原理,则该反应中另一产物应该为氯化氢,其化学式为HCl;
(2) H3PO3 ![]() H++ H2PO3-
H++ H2PO3-
起始时各物质浓度(mol/L) 0.10 0 0
反应的各物质的浓度(mol/L)2.5×10-2 2.5×10-2 2.5×10-2
平衡时各物质的浓度(mol/L)0.10-2.5×10-2 2.5×10-2 2.5×10-2
K a1=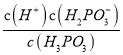 =
= ![]() =8.3×1 0-3 mol/L;
=8.3×1 0-3 mol/L;
(3)亚磷酸具有强还原性,可将Cu2+还原为金属单质,亚磷酸被氧化生成磷酸,则亚磷酸与硫酸铜溶液反应的化学方程式为:H3PO3+CuSO4+H2O=Cu↓+H3PO4+H2SO4;(4)根据Ksp[Ca3(PO4)2]=[c(Ca2+)]3×c(PO43-)=2×10-29,将c(PO43-)=4×10-7mol·L-1代入计算得c(Ca2+)=5×10-6mol·L-1。

 阅读快车系列答案
阅读快车系列答案