题目内容
6.下列叙述正确的是 ( )| A. | H+的摩尔质量是1g | B. | H+的摩尔质量是1g/mol | ||
| C. | H+的摩尔质量是1 | D. | H+的摩尔质量是1mol |
分析 一种物质的摩尔质量在数值上等于该物质的相对原子质量或相对分子质量,且摩尔质量的单位为g/mol,据此分析.
解答 解:A、摩尔质量的单位为g/mol,故氢离子的摩尔质量应为1g/mol,故A错误;
B、一种物质的摩尔质量在数值上等于该物质的相对原子质量或相对分子质量,氢离子的相对原子质量为1,故氢离子的摩尔质量应为1g/mol,故B正确;
C、摩尔质量的单位为g/mol,故氢离子的摩尔质量应为1g/mol,故C错误;
D、摩尔质量的单位为g/mol,故氢离子的摩尔质量应为1g/mol,故D错误.
故选B.
点评 本题考查了摩尔质量的数值和单位,应注意的是摩尔质量的单位为g/mol.

练习册系列答案
 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案
相关题目
16.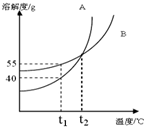 如图是 A、B 两固体物质的溶解度曲线,在t1℃时,将25gA和25gB分别加到各有50g水中的甲、乙烧杯中,充分溶解,下列说法错误的是( )
如图是 A、B 两固体物质的溶解度曲线,在t1℃时,将25gA和25gB分别加到各有50g水中的甲、乙烧杯中,充分溶解,下列说法错误的是( )
 如图是 A、B 两固体物质的溶解度曲线,在t1℃时,将25gA和25gB分别加到各有50g水中的甲、乙烧杯中,充分溶解,下列说法错误的是( )
如图是 A、B 两固体物质的溶解度曲线,在t1℃时,将25gA和25gB分别加到各有50g水中的甲、乙烧杯中,充分溶解,下列说法错误的是( )| A. | t1℃时,A、B两物质饱和溶液中溶质的质量分数相同 | |
| B. | 若A物质中混有少量B物质,可用降温结晶方法提纯A | |
| C. | 由t1℃升温至t2℃,甲烧杯里A物质溶液中溶质的质量分数不变 | |
| D. | 由t1℃升温至t2℃,乙烧杯中B物质溶液的质量不变 |
17.二氧化硒( SeO2)是一种氧化剂,其被还原后的单质硒可能成为环境污染物,通过与浓HN03或浓H2S04反应生成SeO2以回收Se.在回收过程中涉及如下化学反应:①SeO2+4KI+4HN03═Se+2I2+4KN03+2H2O;②Se+2H2S04(浓)═2SO2+Se02+2H20;③Se+4HN03(浓)═Se0+4N02+2H20.下列有关叙述正确的是( )
| A. | SeO2、H2S04(浓)、I2的氧化性由强到弱的顺序是H2S04(浓)>SeO2>I2 | |
| B. | 反应①中Se是氧化产物,I2是还原产物 | |
| C. | 反应①中生成0.6 mol I2,转移的电子数目为2.4NA | |
| D. | 反应②、③中等量的Se消耗浓H2S04和浓HN03的物质的量之比为2:1 |
1.在无色的水溶液中能大量共存的一组离子是( )
| A. | Al3+、Na+、Cl-、H+ | B. | H+、Fe2+、ClO-、Cl- | ||
| C. | Na+、Al3+、Cl-、OH- | D. | K+、Ba2+、Cu2+、Cl- |
18.设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A. | 16g CH4含有4NA个电子 | |
| B. | 0.1mol铁和0.1mol铜分别与0.1mol氯气完全反应,转移的电子数均为0.2NA | |
| C. | 标准状况下,11.2L H2O中分子数为0.5NA个 | |
| D. | 0.1mol•L-1 Na2CO3溶液中含有0.2NA个Na+ |