题目内容
7.已知25℃下,Ka(HCOOH)=1.78×10-4,Kb(NH3•H2O)=1.79×10-5.保持25℃不变,向一定体积0.1mol•L-1 的氨水中滴加0.1mol•L-1 的甲酸溶液.在滴加过程中( )| A. | 水的电离常数先增大后减小 | |
| B. | 当氨水和甲酸溶液体积相等时,c(HCOO-)=c(NH4+) | |
| C. | c(NH3•H2O)与c(NH4+)之和始终保持不变 | |
| D. | $\frac{c(N{{H}_{4}}^{+})c(HCO{O}^{-})}{c(N{H}_{3}•{H}_{2}O)c(HCOOH)}$始终保持不变 |
分析 A.电离常数只与温度有关;
B.弱电解质的电离常数越大,其离子的水解程度越小;
C.溶液的体积增大,c(NH3•H2O)与c(NH4+)之和减小;
D.根据NH3•H2O和HCOOH的电离常数分析.
解答 解:A.电离常数只与温度有关,向一定体积0.1mol•L-1 的氨水中滴加0.1mol•L-1 的甲酸溶液,由于温度不变,水的电离常数不变,故A错误;
B.弱电解质的电离常数越大,其离子的水解程度越小,当氨水和甲酸溶液体积相等时,恰好生成甲酸铵,甲酸的电离常数大,则甲酸根离子的水解程度小,则c(HCOO-)>c(NH4+),故B错误;
C.向一定体积0.1mol•L-1 的氨水中滴加0.1mol•L-1 的甲酸溶液,溶液的体积逐渐增大,氨水的总浓度减小,则c(NH3•H2O)与c(NH4+)之和减小,故C错误;
D.一水合氨的电离常数Kb=$\frac{c(N{{H}_{4}}^{+})•c(O{H}^{-})}{c(N{H}_{3}•{H}_{2}O)}$,HCOOH的电离常数Ka=$\frac{c(HCO{O}^{-})•c({H}^{+})}{c(HCOOH)}$,则$\frac{c(N{{H}_{4}}^{+})c(HCO{O}^{-})}{c(N{H}_{3}•{H}_{2}O)c(HCOOH)}$=$\frac{Ka×Kb}{Kw}$,则$\frac{c(N{{H}_{4}}^{+})c(HCO{O}^{-})}{c(N{H}_{3}•{H}_{2}O)c(HCOOH)}$始终不变,故D正确.
故选D.
点评 本题考查了弱电解质的电离,根据电离平衡常数、酸根离子水解程度之间的关系来分析解答,灵活运用守恒思想分析,题目难度中等.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案
相关题目
18.对下列各种溶液中所含离子的判断合理的是( )
| A. | 某无色溶液中可能含:SO42-、Br-、OH-、Ba2+ | |
| B. | 使紫色石蕊试液变红色的溶液中可能含:K+、Na+、Ba2+、HCO3- | |
| C. | 某溶液中,加铝粉有氢气放出,溶液中可能含:K+、Na+、H+、NO3- | |
| D. | 在c(H+)=10-14mol/L的溶液中可能含:Na+、AlO2-、CO32-、SO32- |
18.工业上产生的氮氧化物可用天然气来处理.
Ⅰ.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1
N2(g)+2O2(g)=2NO2(g)△H2
H2O(l)=H2O(g)△H3
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=△H1-△H2+2△H3(用△H1、△H2、△H3)
Ⅱ.在温度为T1℃和T2℃时,分别将0.50molCH4和1.2molNO2充入体积固定的2L密闭容器中,发生上述可逆反应,测得不同时刻的n(CH4)数据如下表:
(1)分析上表中数据,下列说法正确的是BC
A.T1℃、前10min,V(NO2)=0.03mol/(L•min)
B.T1℃、反应达化学平衡状态时,CH4的转化率为80%
C.T2℃、反应在40min时处于平衡状态
D.T1>T2
(2)反应的平衡常数K(T1)>K(T2),△H<0,理由是由表中数据可知,T2时反应速率较大,所以T1<T2;升高温度平衡逆向移动,可知K(T1)>K(T2),所以正反应放热.
(3)T1℃时反应的平衡常数K为3.2.
(4)反应在T1℃下进行,50min时,向平衡后的容器中再通入0.10molCH4和0.40molNO2,在下图中画出恒温,重新达到平衡过程中n(CH4)随时间变化的曲线(只要求画出n(CH4)的变化趋势,不需要准确画出再次平衡后n(CH4).
Ⅲ.NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图.该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-=N2O5.

Ⅰ.已知:CH4(g)+2O2(g)═CO2(g)+2H2O(l)△H1
N2(g)+2O2(g)=2NO2(g)△H2
H2O(l)=H2O(g)△H3
CH4(g)+2NO2(g)=N2(g)+CO2(g)+2H2O(g)△H=△H1-△H2+2△H3(用△H1、△H2、△H3)
Ⅱ.在温度为T1℃和T2℃时,分别将0.50molCH4和1.2molNO2充入体积固定的2L密闭容器中,发生上述可逆反应,测得不同时刻的n(CH4)数据如下表:
| 温度 | 时间/min n/mol | 0 | 10 | 20 | 40 | 50 |
| T1℃ | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
| T2℃ | n(CH4) | 0.50 | 0.30 | 0.18 | 0.15 | 0.15 |
A.T1℃、前10min,V(NO2)=0.03mol/(L•min)
B.T1℃、反应达化学平衡状态时,CH4的转化率为80%
C.T2℃、反应在40min时处于平衡状态
D.T1>T2
(2)反应的平衡常数K(T1)>K(T2),△H<0,理由是由表中数据可知,T2时反应速率较大,所以T1<T2;升高温度平衡逆向移动,可知K(T1)>K(T2),所以正反应放热.
(3)T1℃时反应的平衡常数K为3.2.
(4)反应在T1℃下进行,50min时,向平衡后的容器中再通入0.10molCH4和0.40molNO2,在下图中画出恒温,重新达到平衡过程中n(CH4)随时间变化的曲线(只要求画出n(CH4)的变化趋势,不需要准确画出再次平衡后n(CH4).
Ⅲ.NO2、O2和熔融NaNO3可制作燃料电池,其原理见下图.该电池在使用过程中石墨Ⅰ电极上生成氧化物Y,其电极反应式为NO2-e-+NO3-=N2O5.

15.有关电解质溶液的叙述,下列说法中正确的是( )
| A. | 0.2 mol•L-1氨水中,c(OH-)与c(NH4+)相等 | |
| B. | 0.1 mol/L的Na2S溶液中,c(OH-)=c(H+)+c(HS-)+c(H2S) | |
| C. | pH=3的一元酸和pH=11的一元碱等体积混和后的溶液中一定是c(OH-)=c(H+) | |
| D. | 10mL0.02mol•L-1HCl溶液与10mL0.02mol•L-1Ba(OH)2溶液充分混合,若混合后溶液的体积为20 mL,则溶液的pH=12 |
2.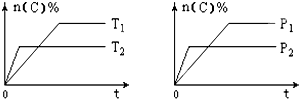 可逆反应aA(g)+bB(s)?cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )
可逆反应aA(g)+bB(s)?cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )
 可逆反应aA(g)+bB(s)?cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )
可逆反应aA(g)+bB(s)?cC(g)+dD(g),其他条件不变,C的物质的量分数和温度(T)或压强(P)关系如图,其中正确的是( )| A. | 升高温度,平衡向逆反应方向移动 | |
| B. | 使用催化剂,C的物质的量分数增加 | |
| C. | 化学方程式系数a>c+d | |
| D. | 根据图象无法确定改变温度后平衡移动方向 |
12.根据碘与氢气反应的热化学方程式,下列判断正确的是( )
①I2(g)+H2(g)?2HI(g)△H=-9.48kJ/mol
②I2(s)+H2(g)?2HI(g)△H=+26.48kJ/mol.
①I2(g)+H2(g)?2HI(g)△H=-9.48kJ/mol
②I2(s)+H2(g)?2HI(g)△H=+26.48kJ/mol.
| A. | 254gI2(g)中通入2gH2(g),反应放热9.48kJ | |
| B. | 当反应②吸收52.96kJ热量时转移2mole- | |
| C. | 反应②的反应物总能量比反应①的反应物总能量低 | |
| D. | 1mol固态碘与1mol气态碘多了17.00kJ能量 |
19.实验是化学研究的一种重要手段,下列有关实验的描述,合理的是( )
| 实验目的 | 主要仪器 | 试剂 | |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、0.1000mol•L-1盐酸 |
| A. | A | B. | B | C. | C | D. | D |
17.向一定量的Fe,FeO,Fe2O3的混合物中加入10mL 18mol•L-1硫酸,加热使之反应,最后硫酸恰好将固体混合物溶解,反应过程中共得到气体2240mL(标准状况下),向所得溶液中滴加KSCN溶液未见红色出现,下列说法中不正确的是( )
| A. | 溶解所得溶液为FeSO4溶液 | |
| B. | 在反应过程中浓硫酸表现了氧化性和酸性 | |
| C. | 原混合物中n(Fe)=n(Fe2O3)+0.1mol | |
| D. | 若用足量碳还原原混合物可得到10.08g铁单质 |