题目内容
19.实验是化学研究的一种重要手段,下列有关实验的描述,合理的是( )| 实验目的 | 主要仪器 | 试剂 | |
| A | 分离Br2和CCl4混合物 | 分液漏斗、烧杯 | Br2和CCl4混合物、蒸馏水 |
| B | 鉴别葡萄糖和蔗糖 | 试管、烧杯、酒精灯 | 葡萄糖溶液、蔗糖溶液、银氨溶液 |
| C | 实验室制取H2 | 试管、带导管的橡皮塞 | 锌粒、稀HNO3 |
| D | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 | NaOH溶液、0.1000mol•L-1盐酸 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.Br2和CCl4混合物不分层;
B.葡萄糖含-CHO,具有还原性,而蔗糖不具有;
C.锌粒、稀HNO3反应生成NO,不生成氢气;
D.中和滴定实验,需要胶头滴管滴加指示剂.
解答 解:A.Br2和CCl4混合物不分层,不能利用分液漏斗分离,应选蒸馏装置及相应仪器分离,故A错误;
B.葡萄糖含-CHO,具有还原性,而蔗糖不具有,则选银氨溶液后水浴加热,需要仪器为试管、烧杯、酒精灯,产生银镜的为葡萄糖,故B正确;
C.锌粒、稀HNO3反应生成NO,不生成氢气,制备氢气应选稀硫酸,故C错误;
D.中和滴定实验,需要胶头滴管滴加指示剂,则仪器缺少胶头滴管,试剂缺酸碱指示剂,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,涉及混合物分离提纯、物质检验、气体的制备及中和滴定实验等,把握物质的性质、实验技能为解答的关键,侧重分析与实验能力的考查,综合性较强,题目难度不大.

练习册系列答案
相关题目
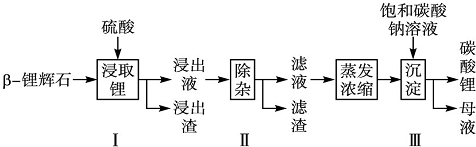
9.碳酸锂广泛应用于陶瓷和医药等领域.以β锂辉石(主要成分为Li2O•Al2O3•4SiO2,含有少量能溶于酸的铁的化合物和镁的化合物)为原料制备Li2CO3的工艺流程如下:
提示信息:
①下列四种离子完全沉淀时溶液pH值如下表:
②Li2SO4、LiOH常温下易溶于水,Li2CO3微溶于水.
回答下列问题:
(1)步骤Ⅰ前,β锂辉石要粉碎成细颗粒的目的是增加样品与H2SO4的接触面积,加快化学反应速率.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO${\;}_{4}^{2-}$,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石(填“石灰石”“氯化钙”或“稀硫酸”)以调节溶液的pH到6.0~6.5,可以除去的离子有Al3+、Fe3+,然后分离得到浸出液.
(3)步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有Fe2+、Mg2+、Ca2+.
(4)步骤Ⅲ中,生成沉淀的离子方程式为2Li++CO32-=Li2CO3↓.
提示信息:
①下列四种离子完全沉淀时溶液pH值如下表:
| 金属离子 | 完全沉淀pH |
| Fe2+ | 9.7 |
| Mg2+ | 12.4 |
| Fe3+ | 3.2 |
| Al3+ | 5.2 |
回答下列问题:
(1)步骤Ⅰ前,β锂辉石要粉碎成细颗粒的目的是增加样品与H2SO4的接触面积,加快化学反应速率.
(2)步骤Ⅰ中,酸浸后得到的酸性溶液中含有Li+、SO${\;}_{4}^{2-}$,另含有Al3+、Fe3+、Fe2+、Mg2+、Ca2+、Na+等杂质,需在搅拌下加入石灰石(填“石灰石”“氯化钙”或“稀硫酸”)以调节溶液的pH到6.0~6.5,可以除去的离子有Al3+、Fe3+,然后分离得到浸出液.
(3)步骤Ⅱ中,将适量的H2O2溶液、石灰乳和Na2CO3溶液依次加入浸出液中,可除去的杂质金属离子有Fe2+、Mg2+、Ca2+.
(4)步骤Ⅲ中,生成沉淀的离子方程式为2Li++CO32-=Li2CO3↓.

10. 25℃时,三种酸的电离常数为:
25℃时,三种酸的电离常数为:
请回答下列问题:
(1)物质的量浓度为0.1mol/L的下列物质:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3;pH由大到小的顺序是:a>b>d>c(填编号)
(2)常温下0.1mol/L的CH3COOH在水中约有1%发生电离,其溶液的pH=3,将该溶液加蒸馏水稀释,在稀释过程中,下列表达式的数据变大的是:BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$
C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加蒸馏水稀释至1 000mL,稀释过程pH变化如图;则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液水电离出来的c(H+)(填“大于”、“等于”或“小于”).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)-c(Na+)=9.9×10-7mol/L(填准确数值).
 25℃时,三种酸的电离常数为:
25℃时,三种酸的电离常数为:| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数K | 1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
(1)物质的量浓度为0.1mol/L的下列物质:a.Na2CO3、b.NaClO、c.CH3COONa、d.NaHCO3;pH由大到小的顺序是:a>b>d>c(填编号)
(2)常温下0.1mol/L的CH3COOH在水中约有1%发生电离,其溶液的pH=3,将该溶液加蒸馏水稀释,在稀释过程中,下列表达式的数据变大的是:BD.
A.c(H+) B.$\frac{c({H}^{+})}{c(C{H}_{3}COOH)}$
C.c(H+)•c(OH-) D.$\frac{c(O{H}^{-})}{c({H}^{+})}$
(3)体积为10mL pH=2的醋酸溶液与一元酸HX分别加蒸馏水稀释至1 000mL,稀释过程pH变化如图;则HX的电离平衡常数大于(填“大于”、“等于”或“小于”)醋酸的电离平衡常数;稀释后,HX溶液中水电离出来的c(H+)大于醋酸溶液水电离出来的c(H+)(填“大于”、“等于”或“小于”).
(4)25℃时,CH3COOH与CH3COONa的混合溶液,若测得混合液pH=6,则溶液中:c(CH3COO-)-c(Na+)=9.9×10-7mol/L(填准确数值).
7.已知25℃下,Ka(HCOOH)=1.78×10-4,Kb(NH3•H2O)=1.79×10-5.保持25℃不变,向一定体积0.1mol•L-1 的氨水中滴加0.1mol•L-1 的甲酸溶液.在滴加过程中( )
| A. | 水的电离常数先增大后减小 | |
| B. | 当氨水和甲酸溶液体积相等时,c(HCOO-)=c(NH4+) | |
| C. | c(NH3•H2O)与c(NH4+)之和始终保持不变 | |
| D. | $\frac{c(N{{H}_{4}}^{+})c(HCO{O}^{-})}{c(N{H}_{3}•{H}_{2}O)c(HCOOH)}$始终保持不变 |
14.下列现象及结论均正确的是( )
| 现象 | 结论 | |
| A | 向Na2O2与水反应完的溶液中,滴加石蕊试液,溶液先变蓝后褪色 | Na2O2与水反应后的溶液呈碱性,且有少量的Na2O2剩余,而氧化石蕊使其褪色 |
| B | 将盐酸与NaHCO3反应生成的CO2气体,直接通入Na2SiO3溶液中出现浑浊 | 说明碳的非金属性强于硅 |
| C | Na2S溶液与Na2SO3溶液混合后出现浑浊 | 发生反应的离子方程式为: 2S2-+SO32-+3H2O═3S↓+6OH- |
| D | 用饱和食盐水吸收氯气中混有的HCl气体,出现白色浑浊 | 白色浑浊为析出的氯化钠晶体 |
| A. | A | B. | B | C. | C | D. | D |
11.如表有关实验的解释或结论不正确的是( )
| 选项 | 实验操作 | 现象 | 解释或结论 |
| A | 某溶液加CCl4,振荡、静置 | 下层溶液显紫色 | 原溶液中一定有I2 |
| B | 向样品溶液中先滴加过量的稀盐酸,再滴加BaCl2溶液 | 滴加稀盐酸无现象,滴加BaCl2后出现白色沉淀. | 说明样品溶液中一定含有SO42- |
| C | 向某溶液中加入硝酸银,再加入稀硝酸 | 有白色沉淀 | 原溶液中有Cl- |
| D | 向某溶液中加入稀硫酸 | 生成无色气体 | 说明原溶液中一定有CO32- |
| A. | A | B. | B | C. | C | D. | D |
8.下列各选项中,前者属于电解质,后者属于非电解质的是( )
| A. | NaOH、氯气 | B. | 盐酸、蔗糖 | C. | 熔融NaCl、酒精 | D. | 二氧化碳、BaSO4 |
9.下列说法不正确的是( )
| A. | 1mol氢 | B. | 1mol氧原子 | C. | 1molH | D. | 1molNaOH |