题目内容
【题目】二茂铁[(C5H5)2Fe]是由一个二价铁离子和2个环戊烯基负离子构成,它的发现可以说是有机金属化合物研究中具有里程碑意义的事件,它开辟了金属有机化合物研究的新领域。已知:二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂。下列说法正确的是( )
A. 二茂铁属于离子晶体
B. 在二茂铁结构中,C5H5-与Fe2+之间形成的化学键类型是离子键
C. 已知:环戊二烯的结构式为: ,则其中碳环上有2个π键和5个σ键
,则其中碳环上有2个π键和5个σ键
D. 二价铁离子的基态电子排布式为:[Ar]3d44s2
【答案】C
【解析】
A. 熔沸点较低的晶体一般为分子晶体;
B. 含有孤电子对和空轨道的原子之间易形成配位键;
C. 依据共价键存在形式作答;
D. 根据构造原理写出其核外电子排布式。
A. 依据题意,二茂铁熔点是173 ℃(在100 ℃时开始升华),沸点是249 ℃,不溶于水,易溶于苯、乙醚等非极性溶剂,熔沸点较低的晶体一般为分子晶体,所以可推断二茂铁晶体为分子晶体,A项错误;
B. 碳原子含有孤电子对,铁含有空轨道,所以碳原子和铁原子之间形成配位键,B项错误;
C. 共价双键中含1个π键和1个σ键,共价单键中含1个σ键,则根据环戊二烯的结构式可知,碳环上有2个π键和5个σ键,C项正确;
D. 铁的原子序数是26,其核外电子数是26,铁原子失2个电子生成亚铁离子,根据构造原理知亚铁离子的核外电子排布式为:[Ar]3d6,D项错误;
答案选C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】CH4-CO2催化重整不仅可以得到合成气(CO和H2),还对温室气体的减排具有重要意义。回答下列问题:
(1)CH4-CO2催化重整反应为:CH4(g)+CO2(g)=2CO(g)+2H2(g)。
已知:C(s)+2H2(g)=CH4(g) ΔH=-75 kJ·mol1
C(s)+O2(g)=CO2(g) ΔH=-394 kJ·mol1
C(s)+1/2O2(g)=CO(g) ΔH=-111 kJ·mol1
该催化重整反应的ΔH==______ kJ·mol1。有利于提高CH4平衡转化率的条件是____(填标号)。
A.高温低压 B.低温高压 C.高温高压 D.低温低压
某温度下,在体积为2 L的容器中加入2 mol CH4、1 mol CO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_______mol2·L2。
(2)反应中催化剂活性会因积碳反应而降低,同时存在的消碳反应则使积碳量减少。
相关数据如下表:
积碳反应 CH4(g)=C(s)+2H2(g) | 消碳反应 CO2(g)+C(s)=2CO(g) | ||
ΔH/(kJ·mol1) | 75 | 172 | |
活化能/ (kJ·mol1) | 催化剂X | 33 | 91 |
催化剂Y | 43 | 72 | |
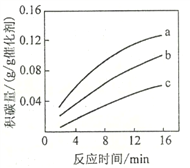
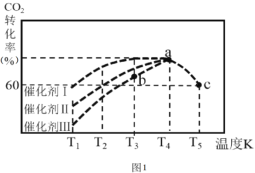
①由上表判断,催化剂X____Y(填“优于”或“劣于”),理由是_________________。在反应进料气组成、压强及反应时间相同的情况下,某催化剂表面的积碳量随温度的变化关系如图所示。升高温度时,下列关于积碳反应、消碳反应的平衡常数(K)和速率(v)的叙述正确的是________填标号)。

A.K积、K消均增加 B.v积减小,v消增加
C.K积减小,K消增加 D.v消增加的倍数比v积增加的倍数大
②在一定温度下,测得某催化剂上沉积碳的生成速率方程为v=k·p(CH4)·[p(CO2)]-0.5(k为速率常数)。在p(CH4)一定时,不同p(CO2)下积碳量随时间的变化趋势如图所示,则pa(CO2)、pb(CO2)、pc(CO2)从大到小的顺序为________________。