题目内容
【题目】(1)实验室用下图所示装置制备少量乙酸乙酯。
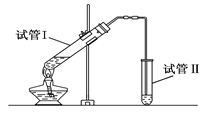
①写出制备乙酸乙酯的化学方程式_______________________。
②试管Ⅱ中盛的试剂是____________________________。
③若要把制得的乙酸乙酯分离出来,应采用的实验操作是________。
(2)已知乳酸的结构简式为![]() 。试回答:
。试回答:
①乳酸分子中含有________和_________两种官能团(写名称);
②乳酸与足量金属钠反应的化学方程式为_____________________________;
【答案】![]() 饱和Na2CO3溶液 分液 羟基 羧基
饱和Na2CO3溶液 分液 羟基 羧基 ![]() + 2Na
+ 2Na![]()
![]() + H2↑
+ H2↑
【解析】
(1)①实验室利用乙酸和乙醇制备乙酸乙酯,反应的化学方程式为![]() ;
;
②生成的乙酸乙酯中含有乙酸和乙醇,可以用饱和碳酸钠溶液除去,即试管Ⅱ中盛的试剂是饱和Na2CO3溶液;
③乙酸乙酯不溶于水,则要把制得的乙酸乙酯分离出来,应采用的实验操作是分液;
(2)①根据结构简式可判断乳酸分子中含有羟基和羧基两种官能团;
②羟基和羧基均能与钠反应,则乳酸与足量金属钠反应的化学方程式为:
![]() + 2Na
+ 2Na![]()
![]() + H2↑。
+ H2↑。

练习册系列答案
 金牌教辅培优优选卷期末冲刺100分系列答案
金牌教辅培优优选卷期末冲刺100分系列答案
相关题目