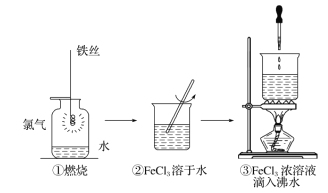
题目内容
【题目】某溶液可能含有K+、NH4+、Mg2+、Fe2+、Fe3+、SO42-、Br-、Cl-、CO32-中的若干种,离子浓度均相等,实验及现象如下:
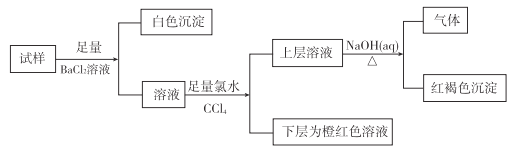
下列判断正确的是
A. 白色沉淀是BaSO4和BaCO3
B. 原溶液存在Fe3+,不存在Fe2+
C. 若原溶液存在Fe3+,必然存在Cl-,无K+
D. 原溶液不存在CO32-、Mg2+、K+、C1-
【答案】C
【解析】加入足量的BaCl2溶液,出现白色沉淀,此沉淀是BaCO3、BaSO4至少一种,溶液中加入氯水和CCl4,下层为橙红色溶液,生成Br2,即原溶液种含有Br-,上层溶液中加入NaOH溶液,产生气体,此气体为NH3,说明原溶液中含有NH4+,产生红褐色沉淀,说明原溶液含有Fe3+、Fe2+至少一种,根据离子共存,原容易一定不存在CO32-,即白色沉淀为BaSO4,A、根据上述分析,白色沉淀为BaSO4,故A错误;B、氯水具有强氧化性,能把Fe2+氧化成Fe3+,同样产生红褐色沉淀,因此原溶液中可能存在Fe2+,故B错误;C、根据上述分析一定没有的离子是CO32-,一定存在的离子是SO42-和NH4+,如果存在Fe3+,根据电荷守恒,以及离子浓度相等,假设离子浓度为1mol·L-1,阳离子所带电荷4,阴离子所带电荷2,因此一定含有Cl-,不含有K+,故C正确;D、根据选项D分析,原溶液中含有Cl-,故D错误。

练习册系列答案
 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案
相关题目