题目内容
如下图中①—11分别代表有关反应物中的一种物质,请填写以下空白。
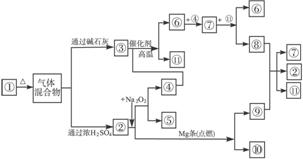
(1)①③④的化学式分别是___________、___________、___________。
(2)⑧与⑨反应的化学方程式是________________________________________________。
(3)②与Mg条(点燃)反应的化学方程式为:__________________________________。
(1)NH4HCO3 NH3 O2
(2)C+4HNO3====4NO2↑+CO2↑+2H2O
(3)CO2+2Mg![]() C+2MgO
C+2MgO
解析:
由②+Mg![]() ⑨+⑩,想到中学化学的典型反应CO2+2Mg====C+2MgO知②为CO2(突破口)
⑨+⑩,想到中学化学的典型反应CO2+2Mg====C+2MgO知②为CO2(突破口)
由:②+Na2O2![]() ④+⑤,且②为CO2知④、⑤为Na2CO3和 O2
④+⑤,且②为CO2知④、⑤为Na2CO3和 O2
由:③+④![]() ⑥+?B11?,知④为O2则⑤为Na2CO3,③为NH3。
⑥+?B11?,知④为O2则⑤为Na2CO3,③为NH3。
其余依次推出:①为(NH4)2CO3或NH4HCO3,⑥为NO,⑦为NO2,
⑧为HNO3,⑨为C,⑩为MgO,?B11?为H2O。

练习册系列答案
相关题目
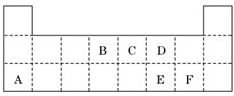
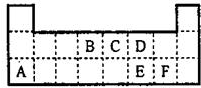 如图为元素周期表的一部分.表中所列的字母分别代表某一元素.
如图为元素周期表的一部分.表中所列的字母分别代表某一元素.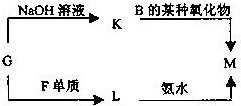
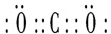

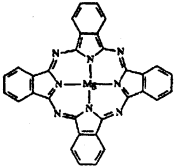 能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.
能源问题日益成为制约国际社会经济发展的瓶颈,越来越多的国家开始实行“阳光计划”,开发太阳能资源,寻求经济发展的新动力.