题目内容
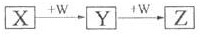 (2011?百色模拟)X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略),下列说法不正确的是( )
(2011?百色模拟)X、Y、Z、W均为中学化学的常见物质,一定条件下它们之间有如图转化关系(其它产物已略),下列说法不正确的是( )分析:A.根据假设去验证各个反应;
B.根据题意推知氢氧化物Y具有酸性,从而推知其他物质;
C.根据W具有强氧化性去逐步分析;
D.根据W是氧气,推测X可能为什么物质,进而得出其他物质.
B.根据题意推知氢氧化物Y具有酸性,从而推知其他物质;
C.根据W具有强氧化性去逐步分析;
D.根据W是氧气,推测X可能为什么物质,进而得出其他物质.
解答:解:A.如果W是Fe,Z是FeCl2,则Y必是FeCl3,发生的化学反应是2FeCl2+Cl2═2FeCl3,则X是盐酸,符合题干要求,故A正确;
B.若W是氢氧化钠,说明X能连续与氢氧化钠反应,即Y应是氢氧化物,Y能与氢氧化钠继续反应,说明氢氧化物Y具有酸性,则Y必是氢氧化铝,则X必是含有Al3+的溶液,Al3+水解使溶液呈酸性.Z是ALO2-,Al3+的溶液和ALO2-溶液混合生成氢氧化铝沉淀,故B正确;
C.若X是镁的单质,则Y与Z中的元素应具有可变化合价,镁无变价,故C错误;
D.若X是甲醇,甲醇应是能被氧气连续氧化的物质,CH3OH
HCHO
HCOOH,CH3OH和COOH的相对原子质量相差14,故D正确;
故选C.
B.若W是氢氧化钠,说明X能连续与氢氧化钠反应,即Y应是氢氧化物,Y能与氢氧化钠继续反应,说明氢氧化物Y具有酸性,则Y必是氢氧化铝,则X必是含有Al3+的溶液,Al3+水解使溶液呈酸性.Z是ALO2-,Al3+的溶液和ALO2-溶液混合生成氢氧化铝沉淀,故B正确;
C.若X是镁的单质,则Y与Z中的元素应具有可变化合价,镁无变价,故C错误;
D.若X是甲醇,甲醇应是能被氧气连续氧化的物质,CH3OH
| O2 |
| O2 |
故选C.
点评:本题根据一个反应线索,去进行各种可能性的设问,考查了学生对元素及其化合物知识的掌握程度,具有较大的难度,解答这类题目的关键在于学生要掌握系统的相关知识

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
 (2011?百色模拟)大豆异黄酮(结构如图)是一种近年来引起营养与医学界广泛关注的物质,它对于人体健康有着重要的作用.关于大豆异黄酮的叙述错误的是( )
(2011?百色模拟)大豆异黄酮(结构如图)是一种近年来引起营养与医学界广泛关注的物质,它对于人体健康有着重要的作用.关于大豆异黄酮的叙述错误的是( )