题目内容
【题目】2SO2(g)+O2(g)![]() 2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
2SO3(g)反应过程的能量变化如图所示。已知1 mol SO2(g)氧化为1 mol SO3(g)的ΔH=-99 kJ·mol-1。请回答下列问题:
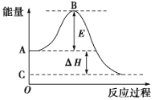
(1)图中A点表示:________________________________________;C点表示:________________。E的大小对该反应的反应热________(填“有”或“无”)影响。
(2)图中ΔH=________kJ·mol-1。
【答案】反应物的总能量生成物的总能量无-198
【解析】
(1)A、C分别表示反应物的总能量、生成物的总能量,E为活化能,活化能的大小与反应热无关;
(2)根据参加反应SO2的物质的量之比等于对应的ΔH之比计算。
(1)根据图像可知图中A、C分别表示反应物的总能量、生成物的总能量,E为反应物活化能,反应热可表示为反应物和生成物活化能的大小之差,因此活化能的大小与反应热无关;
(2)由于1 mol SO2氧化为1 mol SO3的ΔH=-99 kJ·mol-1,所以2mol SO2氧化为2mol SO3的ΔH=-198 kJ·mol-1。

练习册系列答案
 全优冲刺100分系列答案
全优冲刺100分系列答案 英才点津系列答案
英才点津系列答案
相关题目