题目内容
(1)写出下列物质在水溶液中的电离方程式氢氧化钡
(2)写出下列反应的离子方程式或化学方程式:
硫酸溶液与澄清的石灰水混合
Ba(OH)2=Ba2++2OH-
Ba(OH)2=Ba2++2OH-
硫酸铝Al2(SO4)3=2 Al3++3SO42-
Al2(SO4)3=2 Al3++3SO42-
(2)写出下列反应的离子方程式或化学方程式:
硫酸溶液与澄清的石灰水混合
Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O.
Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O.
;碳酸氢钠溶液与稀盐酸混合H++HCO3-=H2O+CO2↑
H++HCO3-=H2O+CO2↑
;MgO+2H+═Mg2++H2OMgO+2HCl═MgCl2+H2O
MgO+2HCl═MgCl2+H2O
.分析:(1)强电解质的电离不可逆,用“═”,弱电解质的电离可逆,用“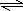 ”,离子团不能拆开写.
”,离子团不能拆开写.
(2)根据化学方程式书写其离子方程式;
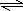 ”,离子团不能拆开写.
”,离子团不能拆开写.(2)根据化学方程式书写其离子方程式;
解答:解:(1)Ba(OH)2、Al2(SO4)3均能完全电离,电离方程式分别为Ba(OH)2=Ba2++2OH-,Al2(SO4)3=2Al3++3SO42-,故答案为:Ba(OH)2=Ba2++2OH-;Al2(SO4)3=2Al3++3SO42-,
(2)硫酸溶液和澄清的石灰水混合生成硫酸钙沉淀和水,反应的离子方程式为:Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O;
碳酸氢钠溶液与稀盐酸混合生成氯化钠、水和二氧化碳,反应的离子方程式为:H++HCO3-=H2O+CO2↑;
离子方程式MgO+2H+═Mg2++H2O表示氧化镁与强酸反应生成可溶性镁盐和水,反应的化学方程式为:
MgO+2HCl═MgCl2+H2O.
(2)硫酸溶液和澄清的石灰水混合生成硫酸钙沉淀和水,反应的离子方程式为:Ca2++2OH-+2H++SO42-=CaSO4↓+2H2O;
碳酸氢钠溶液与稀盐酸混合生成氯化钠、水和二氧化碳,反应的离子方程式为:H++HCO3-=H2O+CO2↑;
离子方程式MgO+2H+═Mg2++H2O表示氧化镁与强酸反应生成可溶性镁盐和水,反应的化学方程式为:
MgO+2HCl═MgCl2+H2O.
点评:本题考查了学生电离方程式、离子方程式的书写,注意离子团不能拆开这一细节以及在离子方程式中能拆的物质有强酸、强碱和可溶性盐.

练习册系列答案
相关题目