题目内容
【题目】某学生用0.200 0 mol·L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作如下:
①用蒸馏水洗涤碱式滴定管,并立即注入NaOH溶液至“0”刻度线以上;
②固定好滴定管并使滴定管尖嘴处充满液体;
③调节液面至“0”或“0”刻度线以下,并记下读数;
④移取20.00 mL待测液注入洁净的还存有少量蒸馏水的锥形瓶中,并加入3滴酚酞溶液;
⑤用标准液滴定至终点,记下滴定管液面读数。
请回答下列问题:
(1)以上步骤有错误的是______(填编号)。若测定结果偏高,其原因可能是________(填字母)。
A.配制标准溶液的固体NaOH中混有KOH杂质
B.滴定终点读数时,仰视滴定管的刻度,其他操作正确
C.盛装未知液的锥形瓶用蒸馏水洗过后再用未知液润洗
D.所配的标准NaOH溶液物质的量浓度偏大
(2)判断滴定终点的现象是_____________________________________。
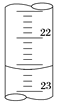
(3)如图是某次滴定时的滴定管中的液面,其读数为________mL。
(4)根据下列数据,请计算待测盐酸的浓度:________mol·L-1。
滴定次数 | 待测体积(mL) | 标准烧碱溶液体积(mL) | |
滴定前读数 | 滴定后读数 | ||
第一次 | 20.00 | 0.40 | 20.40 |
第二次 | 20.00 | 2.00 | 24.10 |
第三次 | 20.00 | 4.00 | 24.00 |
【答案】① ABC 滴入最后一滴NaOH溶液时,溶液刚好由无色变为粉红色,且半分钟内不恢复原色 22.60 0.2000
【解析】
本题考查酸碱中和滴定实验,中和滴定实验的步骤是
滴定前的准备:
滴定管:查漏→洗涤→润洗→装液→调液面→记录,锥形瓶:注液体→记体积→加指示剂
滴定:眼睛注视锥形瓶溶液颜色变化
终点判断:
数据处理:
(1)根据酸碱中和滴定的判断,步骤错误是①,没有用待盛液润洗;根据c待=c标×V标/V待
A、等质量的NaOH和KOH配制一定物质的量浓度的溶液,KOH的物质的量浓度小于NaOH的物质的量浓度,如果配制溶液中固体NaOH中混有KOH,标准溶液的物质的量浓度偏低,滴定时,消耗溶液的体积偏大, 故所测结果偏高,故A符合题意;
B、滴定管刻度从上到下增大,滴定终点时,仰视读数,所计算出消耗标准液的体积增大,即所测结果偏高,故B符合题意;
C、此操作得出消耗标准液的体积增大,所测结果偏高,故C符合题意;
D、NaOH浓度偏高,消耗标准液的体积减小,所测结果将偏低,故D不符合题意;
(2)滴定终点:滴入最后一滴NaOH溶液时,溶液刚好由无色变为粉红色,且半分钟内不恢复原色;
(3)根据图示,读数为22.60mL;
(4)三次消耗标准液的体积分别为20.00、22.10、20.00,第二次消耗的体积与其余相差太多,删去,两次平均消耗标准液的体积为20.00mL,c(HCl)=20.00×10-3×0.2000/(20.00×10-3)mol·L-1=0.2000mol·L-1。

 阅读快车系列答案
阅读快车系列答案【题目】焦炭是重要的工业原材料。
(1)已知在一定温度下,C(s)+CO2(g) ![]() 2CO(g) 平衡常数K1;C(s)+H2O(g)
2CO(g) 平衡常数K1;C(s)+H2O(g) ![]() CO(g)+H2(g) 平衡常数K2 ;CO(g)+H2O(g)
CO(g)+H2(g) 平衡常数K2 ;CO(g)+H2O(g) ![]() H2(g)+CO2(g) 平衡常数K。则K、K1、K2,之间的关系是__________。
H2(g)+CO2(g) 平衡常数K。则K、K1、K2,之间的关系是__________。
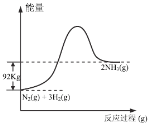
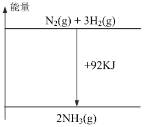
(2)用焦炭还原NO的反应为:2NO(g)+ C(s)![]() N2(g) + CO2(g) ΔH,向容积均为1L的甲、乙、丙三个恒温(反应温度分别为400℃、T ℃、400℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
N2(g) + CO2(g) ΔH,向容积均为1L的甲、乙、丙三个恒温(反应温度分别为400℃、T ℃、400℃)容器中分别加入足量的焦炭和一定量的NO,测得各容器中n(NO)随反应时间t的变化情况如下表所示:
t/min | 0 | 40 | 80 | 120 | 160 |
n(NO)(甲容器)/mol | 2.00 | 1.50 | 1.10 | 0.80 | 0.80 |
n(NO)(乙容器)/mol | 2.00 | 1.45 | 1.00 | 1.00 | 1.00 |
n(NO)(丙容器)/mol | 1.00 | 0.80 | 0.65 | 0.53 | 0.45 |
①甲容器中,0~40 min内用NO的浓度变化表示的平均反应速率v(NO)=_____________ ;
②该反应的平衡常数表达式为__________________;400℃,该反应的平衡常数为_______;
③乙容器的反应温度T____400 ℃(填“>”“<”或“=”)
④丙容器达到平衡时,NO的转化率为___________;平衡时CO2的浓度为________。
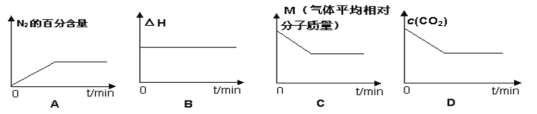
⑤在恒容密闭容器中加入焦炭并充入NO气体,下列图像正确且能说明反应达到平衡状态的是___。