题目内容
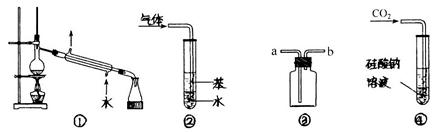
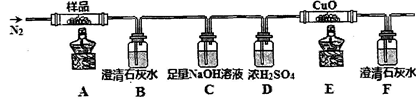
某研究性学习小组的同学想通过下图实验装置探究SO2与Na2O2反应的产物。(夹持装置已略去,装置的气密性良好)
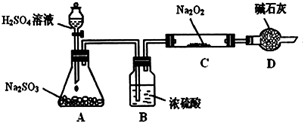
Ⅰ.实验中装置B可吸收水分,干燥SO2气体,其目的是:_________________________。
装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是:_________________。
Ⅱ.对C中固体产物提出如下假设:(假设Na2O2已全部反应)
假设1:__________。 假设2:只有Na2SO4; 假设3:既有Na2SO3又有Na2SO4。
(1)甲同学认为SO2与Na2O2的反应不同于CO2,应为假设2成立,请据此写出C中所发生反应的化学方程式:_____________________。
(2)若假设2成立,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:C中固体产物只有Na2SO4。该方案是否合理?答:__________。(填“是”或“否”)理由是______________________________。
(3)乙同学为证明假设3成立,设计如下实验。
实验步骤和结论为:
①取少量C中固体产物于试管中,加入适量的蒸馏水溶解;
②滴加过量的1mol?L-1BaCl2溶液,若产生白色沉淀,则证明C中固体产物中有_________;
③滴加适量的1mol?L-1稀盐酸,若白色沉淀部分溶解,并产生刺激性气味气体,则证明C中固体产物中有___________________。

Ⅰ.实验中装置B可吸收水分,干燥SO2气体,其目的是:_________________________。
装置D除了吸收过量的SO2,避免污染空气外,还起到的作用是:_________________。
Ⅱ.对C中固体产物提出如下假设:(假设Na2O2已全部反应)
假设1:__________。 假设2:只有Na2SO4; 假设3:既有Na2SO3又有Na2SO4。
(1)甲同学认为SO2与Na2O2的反应不同于CO2,应为假设2成立,请据此写出C中所发生反应的化学方程式:_____________________。
(2)若假设2成立,为确定C中固体产物的成分,甲同学设计如下实验:

得出结论:C中固体产物只有Na2SO4。该方案是否合理?答:__________。(填“是”或“否”)理由是______________________________。
(3)乙同学为证明假设3成立,设计如下实验。
实验步骤和结论为:
①取少量C中固体产物于试管中,加入适量的蒸馏水溶解;
②滴加过量的1mol?L-1BaCl2溶液,若产生白色沉淀,则证明C中固体产物中有_________;
③滴加适量的1mol?L-1稀盐酸,若白色沉淀部分溶解,并产生刺激性气味气体,则证明C中固体产物中有___________________。
Ⅰ.防止水蒸气与Na2O2反应,防止空气中的水和CO2进入玻璃管C。
Ⅱ.假设1:只有Na2SO3
(1)SO2+Na2O2=Na2SO4。(2)否;NO3-在酸性条件下可将BaSO3氧化成BaSO4
或硝酸根在酸性条件下具有强氧化性
(3)②Na2SO3和Na2SO4至少有一种;(2分)
③既有Na2SO3又有Na2SO4。(2分)
Ⅱ.假设1:只有Na2SO3
(1)SO2+Na2O2=Na2SO4。(2)否;NO3-在酸性条件下可将BaSO3氧化成BaSO4
或硝酸根在酸性条件下具有强氧化性
(3)②Na2SO3和Na2SO4至少有一种;(2分)
③既有Na2SO3又有Na2SO4。(2分)
试题分析:Ⅰ、A装置中产生的二氧化硫气体中含有水蒸气,水能和过氧化钠反应生成氢氧化钠和氧气,B装置中浓硫酸具有吸水性,可吸收水蒸气;空气中含有二氧化碳和水蒸气,碱石灰是干燥剂,所以能吸收水分,防止水蒸气的干扰;碱石灰能和二氧化碳反应,防止二氧化碳的干扰,所以装置D的作用是防止空气中的水蒸气和二氧化碳进入C装置与Na2O2反应;Ⅱ、根据题给信息知,假设1:只有Na2SO3; (1)若假设2成立,二氧化硫和过氧化钠反应的方程式为:Na2O2+SO2=Na2SO4 ;(2)硝酸有强氧化性,能把亚硫酸根离子氧化成硫酸根离子,所以该方案不合理;(3)乙同学为证明假设3成立,设计如下实验。实验步骤和结论为:①取少量C中固体产物于试管中,加入适量的蒸馏水溶解;②滴加过量的1mol?L-1BaCl2溶液,若产生白色沉淀,由于硫酸钡和亚硫酸钡均为不溶于水的白色固体,则证明C中固体产物中Na2SO3和Na2SO4至少有一种;③滴加适量的1mol?L-1稀盐酸,若白色沉淀部分溶解,并产生刺激性气味气体,则证明C中固体产物中既有Na2SO3又有Na2SO4。

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目
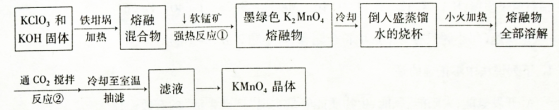


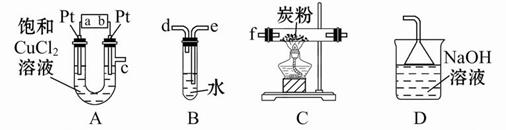
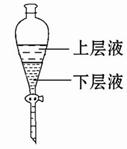
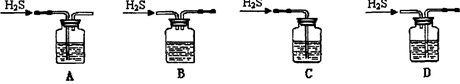
 气体,并防止倒吸
气体,并防止倒吸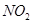 ,如果“b进a出”可用于收集
,如果“b进a出”可用于收集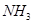
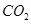 气体,现象是先出现白色沉淀,后变澄清
气体,现象是先出现白色沉淀,后变澄清
 溶液
溶液
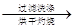 得固体b g
得固体b g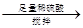
 量气测得气体体积Va mL
量气测得气体体积Va mL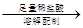 250 mL溶液
250 mL溶液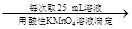 三次平均消耗0.1 mol·L-1酸性KMnO4溶液Vb mL你认为以上方案中 无法确定样品的组成,理由是 。
三次平均消耗0.1 mol·L-1酸性KMnO4溶液Vb mL你认为以上方案中 无法确定样品的组成,理由是 。
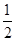 O2 → MnO2 + CO2。
O2 → MnO2 + CO2。