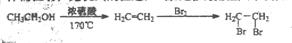题目内容
【化学——选修2:化学与技术】(15分)
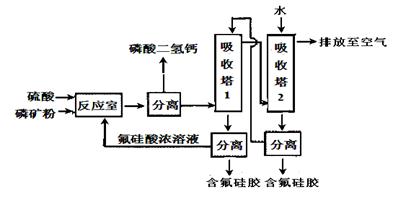
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:

(1)沸腾炉中发生反应的化学方程式为 ;接触室中发生反应的化学方程式是 。
(2)沸腾炉出来的炉气需要精制,如果不经过精制,对SO2催化氧化的影响是
(3)硫酸工业是一种易造成多种形式污染的工业,工业上常采用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理: ;对矿渣的合理利用方法是 。
(4)某工厂用500t 含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是 t。
以黄铁矿(主要成分是FeS2)为原料生产硫酸的工艺流程图如下:

(1)沸腾炉中发生反应的化学方程式为 ;接触室中发生反应的化学方程式是 。
(2)沸腾炉出来的炉气需要精制,如果不经过精制,对SO2催化氧化的影响是
(3)硫酸工业是一种易造成多种形式污染的工业,工业上常采用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理: ;对矿渣的合理利用方法是 。
(4)某工厂用500t 含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是 t。
(15分)(1)4FeS2+11O2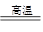 2Fe2O3+8SO2 ; 2SO2+O2
2Fe2O3+8SO2 ; 2SO2+O2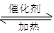 2SO3 (各2分,共4分)
2SO3 (各2分,共4分)
(2)矿尘,砷、硒等化合物导致催化剂中毒,水蒸气对设备和生产有不良影响 (2分)
(3)SO2+2NH3·H2O === (NH4)2SO3+ H2O
(NH4)2SO3+H2SO4=== (NH4)2SO4+SO2↑↑+H2O ;炼铁 (各2分,共6分)
(4)705.6
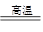 2Fe2O3+8SO2 ; 2SO2+O2
2Fe2O3+8SO2 ; 2SO2+O2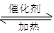 2SO3 (各2分,共4分)
2SO3 (各2分,共4分)(2)矿尘,砷、硒等化合物导致催化剂中毒,水蒸气对设备和生产有不良影响 (2分)
(3)SO2+2NH3·H2O === (NH4)2SO3+ H2O
(NH4)2SO3+H2SO4=== (NH4)2SO4+SO2↑↑+H2O ;炼铁 (各2分,共6分)
(4)705.6
(1)沸腾炉中发生反应的化学方程式为4FeS2+11O2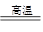 2Fe2O3+8SO2 ;接触室中发生反应的化学方程式为2SO2+O2
2Fe2O3+8SO2 ;接触室中发生反应的化学方程式为2SO2+O2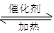 2SO3;
2SO3;
(2)沸腾炉出来的炉气需要精制,如果不经过精制,对SO2催化氧化的影响是矿尘,砷、硒等化合物导致催化剂中毒,水蒸气对设备和生产有不良影响;
(3)硫酸工业是一种易造成多种形式污染的工业,工业上常采用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理SO2+2NH3·H2O === (NH4)2SO3+ H2O;(NH4)2SO3+H2SO4=== (NH4)2SO4+SO2↑↑+H2O ;对矿渣的合理利用方法是炼铁;
(4)某工厂用500t 含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是705.6t;
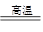 2Fe2O3+8SO2 ;接触室中发生反应的化学方程式为2SO2+O2
2Fe2O3+8SO2 ;接触室中发生反应的化学方程式为2SO2+O2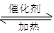 2SO3;
2SO3;(2)沸腾炉出来的炉气需要精制,如果不经过精制,对SO2催化氧化的影响是矿尘,砷、硒等化合物导致催化剂中毒,水蒸气对设备和生产有不良影响;
(3)硫酸工业是一种易造成多种形式污染的工业,工业上常采用氨—酸法进行尾气脱硫,以达到消除污染、废物利用的目的。用化学方程式表示其反应原理SO2+2NH3·H2O === (NH4)2SO3+ H2O;(NH4)2SO3+H2SO4=== (NH4)2SO4+SO2↑↑+H2O ;对矿渣的合理利用方法是炼铁;
(4)某工厂用500t 含硫量为48%的黄铁矿制备硫酸,若在沸腾炉中有2%的FeS2损失,在接触室中SO3的产率为96%,则可得到98%的浓硫酸的质量是705.6t;

练习册系列答案
相关题目
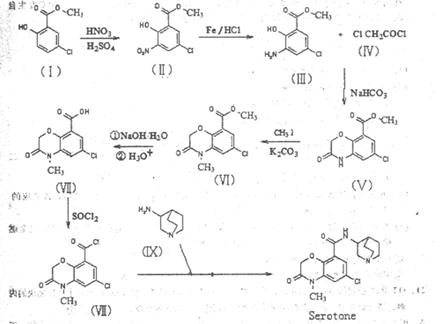
 Ⅴ中NaHCO3gm V
Ⅴ中NaHCO3gm V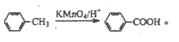
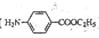 )的合成路线流程图(必要条件需注明,无机试剂任选)。合成路线流程图示例如下:
)的合成路线流程图(必要条件需注明,无机试剂任选)。合成路线流程图示例如下: