��Ŀ����
����Ŀ���л���A������ʳƷ��ҵ����֪9.0g A������O2�г��ȼ�գ������ɵĻ����������ͨ��������Ũ����ͼ�ʯ�ң��ֱ�����5.4g��13.2g��������ʣ������ΪO2 ��
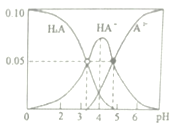
��1��A���ӵ�����ͼ��ͼ��ʾ����ͼ�п�֪����Է���������90����A�ķ���ʽ�� �� 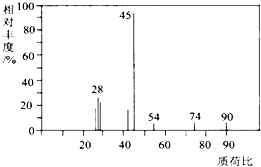
��2��A����NaHCO3��Һ������Ӧ��Aһ�����еĹ����������� ��
��3��A���ӵĺ˴Ź���������4���壬�����֮����1��1��1��3����A�Ľṹ��ʽ�� ��
��4��0.1mol A������Na��Ӧ���ڱ�״���²���H2�������L��
��5��A��һ�������¿ɾۺϵõ�һ�־���������������������ߣ��䷴Ӧ�Ļ�ѧ����ʽ�� ��
���𰸡�
��1��C3H6O3
��2���Ȼ�
��3��CH3CH��OH��COOH
��4��2.24
��5��![]()
���������⣺��1��5.4gˮ�����ʵ���Ϊ�� ![]() =0.3mol��n��H��=0.6 mol��13.2g������̼�����ʵ���Ϊ��
=0.3mol��n��H��=0.6 mol��13.2g������̼�����ʵ���Ϊ�� ![]() =0.3mol��n��C��=n��CO2��=0.3 mol�����л���9.0g��OԪ��������9.0g��0.6g��0.3��12 g=4.8 g��n��O��=
=0.3mol��n��C��=n��CO2��=0.3 mol�����л���9.0g��OԪ��������9.0g��0.6g��0.3��12 g=4.8 g��n��O��= ![]() =0.3 mol����n��C����n��H����n��O��=0.3mol��0.6mol��0.3mol=1��2��1����ʵ��ʽΪCH2O�������ʽΪ��CH2O��n��A����Է�������Ϊ90���ɵ�30n=90����ã�n=3�����л���AΪC3H6O3���ʴ�Ϊ��C3H6O3����2��A����NaHCO3��Һ������Ӧ��Aһ�������Ȼ�����COOH�����ʴ�Ϊ���Ȼ�����3���л���AΪC3H6O3���˴Ź���������4���壬�����֮����1��1��1��3���������4��Hԭ�ӵ���ĿΪ1��1��1��3�������к���1����COOH��1����CH3��1��
=0.3 mol����n��C����n��H����n��O��=0.3mol��0.6mol��0.3mol=1��2��1����ʵ��ʽΪCH2O�������ʽΪ��CH2O��n��A����Է�������Ϊ90���ɵ�30n=90����ã�n=3�����л���AΪC3H6O3���ʴ�Ϊ��C3H6O3����2��A����NaHCO3��Һ������Ӧ��Aһ�������Ȼ�����COOH�����ʴ�Ϊ���Ȼ�����3���л���AΪC3H6O3���˴Ź���������4���壬�����֮����1��1��1��3���������4��Hԭ�ӵ���ĿΪ1��1��1��3�������к���1����COOH��1����CH3��1�� ![]() CH��1����OH���л���A�Ľṹ��ʽΪCH3CH��OH��COOH���ʴ�Ϊ��CH3CH��OH��COOH����4���л���A���Щ�OH�ͩ�COOH��������Na��Ӧ������������Ӧ�Ļ�ѧ����ʽΪ��
CH��1����OH���л���A�Ľṹ��ʽΪCH3CH��OH��COOH���ʴ�Ϊ��CH3CH��OH��COOH����4���л���A���Щ�OH�ͩ�COOH��������Na��Ӧ������������Ӧ�Ļ�ѧ����ʽΪ�� ![]() ���ɷ���ʽ��֪0.1molA������Na��Ӧ��������0.1mol���ڱ�״���²���H2������ǣ�0.1mol��22.4L/mol=2.24L���ʴ�Ϊ��2.24����5���л���A���Щ�OH�ͩ�COOH���ۺϷ�Ӧ�õ������ķ�Ӧ����ʽΪ��
���ɷ���ʽ��֪0.1molA������Na��Ӧ��������0.1mol���ڱ�״���²���H2������ǣ�0.1mol��22.4L/mol=2.24L���ʴ�Ϊ��2.24����5���л���A���Щ�OH�ͩ�COOH���ۺϷ�Ӧ�õ������ķ�Ӧ����ʽΪ�� ![]() ��
��
�ʴ�Ϊ�� ![]() ��
��
��1������Ũ��������5.4gΪˮ����������ʯ������13.2gΪ������̼�����������������غ������Ԫ�ص������������������ʽ���ٽ����Է��������������ʽ����2��A����NaHCO3��Һ������Ӧ��Aһ�������Ȼ�����COOH������3�����ӵĺ˴Ź���������4���壬˵�������к���4��Hԭ�ӣ������֮����1��1��1��3����4��Hԭ�ӵ���Ŀ֮��Ϊ1��1��1��3����Ϸ���ʽ�жϷ��ӽṹ����4������л���Ľṹ�ж����Ƶķ�Ӧ���������������������������5�������л���A�Ľṹ��������Ӧԭ����д��Ӧ����ʽ��

����Ŀ��ijʵ��С����H2O2�ֽ�Ϊ�����о�Ũ�ȡ���������Һ����ԶԷ�Ӧ���ʵ�Ӱ�죬�ڳ����°������·������ʵ�顣
ʵ���� | ��Ӧ�� | ���� |
�� | 10 mL 2% H2O2��Һ | �� |
�� | 10 mL 5% H2O2��Һ | �� |
�� | 10 mL 5% H2O2��Һ | 1 mL 0.1 mol L-1 FeCl3��Һ |
�� | 10 mL 5% H2O2��Һ+����HCl��Һ | 1 mL 0.1 mol L-1 FeCl3��Һ |
�� | 10 mL 5% H2O2��Һ+����NaOH��Һ | 1 mL 0.1 mol L-1 FeCl3��Һ |
��1�������ܼӿ컯ѧ��Ӧ���ʵ�ԭ������
��2��ʵ��ٺ͢ڵ�Ŀ������ʵ��ʱ���ڽϳ�ʱ��û�й۲쵽������������ó����ۡ�������ʾ��ͨ��������H2O2�ȶ������ֽ⡣Ϊ�˴ﵽʵ��Ŀ�ģ����ԭʵ�鷽���ĸĽ�����
��3��д��ʵ��۵Ļ�ѧ��Ӧ����ʽ����
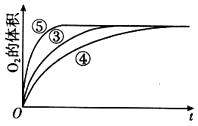
��4��ʵ��ۡ��ܡ����У�������������������ʱ��仯�Ĺ�ϵ��ͼ��������ͼ�ܹ��ó���ʵ���������