��Ŀ����
����Ŀ�����ڹ�ũҵ�������ճ�����������Ҫ��;��

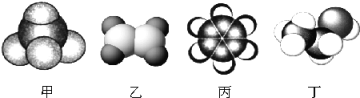
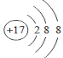
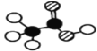
��1����ͼΪ�����Ƶ������ͼ����������պ���ʱ������Ҫ���ż��⣬����Ҫ�õ���ʵ��������____________________��������������ѡ��������������ñ����ĸ��д����
A���ձ� B������ C�������� D�������� E���ƾ��� F��������
����ܷ�����Ӧ�����ӷ���ʽΪ______________________________________________��
������ݲ����ѻ�������ȡ�⣬�����____________________________��
��2���廯��(IBr)�Ļ�ѧ����������±�ص��ʣ�����������������Ӧ���ɽ���±�����ˮ��Ӧ�ķ���ʽΪ��IBr+H2O==HBr+HIO�������й�IBr�������д�����ǣ�________��
A�������廯���۷е�ϸ�
B�������෴Ӧ�У��廯����ǿ������
C����±�ص������ƣ���ˮ��Ӧʱ���廯����������������ǻ�ԭ��
D���廯���NaOH��Һ��Ӧ����NaBr��NaIO��H2O
��3��Ϊʵ���й�������ȱ������Ŀ�ꡣ�������涨ʳ�α���ӵ��Σ����е� ���Ե���أ�KIO3����ʽ���ڡ������������ữ�ĵ⻯�ص�����Һ����ӵ��Σ�����˵����ȷ����___��
A.���������л��ܼ������þƾ���ȡ��ˮ�е�I2
B.����ӵ���ԭ����IO3-+5I-+3H2O=3I2+6OH-
C.��KIO3��Һ�м��뼸�ε�����Һ����Һ����ɫ
D.��ij��ɫ��Һ�м�����ˮ�����Ȼ�̼�������ã��²����ɫ��˵��ԭ��Һ����I-
���𰸡� BDE MnO2+ 4H++2I��== Mn2++I2+2H2O �ѻ����ͺ�ϩ�������I2��Ӧ A C D
��������(1)��������պ�����Ϊ����ļ��ȣ�Ӧ�������н��У���Ҫ�����������żܡ������ǡ������Լ��ƾ��Ƶ�����������������Һ�м��������������ữ��MnO2��Ϊ�˽������������ɵ��ʵ⣬���ӷ���ʽΪMnO2+4H++2I-=Mn2++I2+2H2O��������ݲ����ѻ�������ȡ�⣬�ѻ������к���ϩ����͵ⵥ�ʷ����ӳɷ�Ӧ���ʴ�Ϊ��BDE��MnO2+4H++2I-=Mn2++I2+2H2O���ѻ����ͺ�ϩ�������I2 ��Ӧ��
(2)A�������廯�����ڷ��Ӿ��壬��Է����������۷е㲻�ߣ���A����B��IBr��IԪ�ػ��ϼ�Ϊ+1�ۣ����������ԣ��ںܶѧ��Ӧ��IBr������������B��ȷ��C��IBr��ˮ������ӦԪ�صĻ��ϼ�û�з����仯��Ϊˮ�ⷴӦ����C����D������ˮ�ķ�Ӧ��֪����NaOH��Һ��Ӧ������NaBr��NaIO��ˮ����D��ȷ���ʴ�Ϊ��AC��
(3)A.�ƾ���ˮ���ܣ������þƾ���ȡ��ˮ�е�I2������B. ����غ͵⻯��������Һ�з���������ԭ��Ӧ���ɵⵥ�ʣ��������۱���ɫ����Ӧ�����ӷ���ʽΪ��IO3-+5I-+6H+�T3I2+3H2O������C. KIO3��Һ��û�еⵥ�ʣ����뼸�ε�����Һ����Һ�������ɫ������D. �²���Һ���Ϻ�ɫ��˵�����ɵ⣬��ԭ��Һ�к���I-����ȷ����ѡD��