题目内容
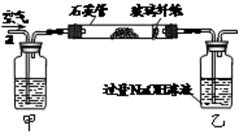
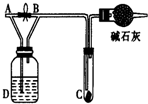 如图所示,A处通入氯气,关闭旋塞B时,C处红色布条无明显的变化,打开旋塞B时,C处红色布条逐渐褪色.由此作出的判断正确的是( )
如图所示,A处通入氯气,关闭旋塞B时,C处红色布条无明显的变化,打开旋塞B时,C处红色布条逐渐褪色.由此作出的判断正确的是( )| A、D中不可能是浓硫酸 | B、D中可以是水 | C、通入的氯气中含有水蒸气 | D、D中可以是饱和食盐水 |
分析:起漂白作用的是次氯酸而不是氯气,所以干燥的氯气不能漂白有色布条,含水蒸气的氯气能使有色布条褪色,A处通入氯气,关闭B阀时,C处红色布条无变化,说明D处可以干燥氯气或吸收氯气.
解答:解:A.浓硫酸具有吸水性,能吸收氯气中的水蒸气而干燥氯气,氯气不能时干燥有色布条褪色,所以A可能是浓硫酸,故A错误;
B.假设D中是水,氯气通过水后带出部分水蒸气,能使有色布条褪色,与实验不符合,故B错误;
C.氯气没有漂白性,次氯酸有漂白性,打开旋塞B时,C处红色布条逐渐褪色,说明氯气中含有水蒸气,故C正确;
D.D中是饱和食盐水时,与选项B原理相同,故D错误;
故选C.
B.假设D中是水,氯气通过水后带出部分水蒸气,能使有色布条褪色,与实验不符合,故B错误;
C.氯气没有漂白性,次氯酸有漂白性,打开旋塞B时,C处红色布条逐渐褪色,说明氯气中含有水蒸气,故C正确;
D.D中是饱和食盐水时,与选项B原理相同,故D错误;
故选C.
点评:本题考查了氯气性质,明确起漂白作用的物质是解题的关键,再根据是否含有水分来分析解答,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目