题目内容
一定条件下,对于可逆反应X(g)+3Y(g) 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是( )
 2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是( )
2Z(g),若X、Y、Z的起始浓度分别为c1、c2、c3(均不为零),达到平衡时,X、Y、Z的浓度分别为0.1 mol/L、0.3 mol/L、0.08 mol/L,则下列判断正确的是( )| A.c1∶c2=3∶1 |
| B.平衡时,Y和Z的生成速率之比为2∶3 |
| C.c1的取值范围为0.04 mol/L<c1<0.14 mol/L |
| D.X、Y的转化率相等 |
D
根据方程式可知,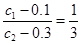 ,解得c1∶c2=1∶3,即二者的起始浓度之比恰好等于相应的化学计量数之比,所以X、Y的转化率相等,A不正确,D正确;反应速率之比是相应的化学计量数之比,所以平衡时,Y和Z的生成速率之比为3∶2,B不正确;如果反应向正反应方向进行,则(c1-0.1)×2=0.08-c3,解得c1<0.14 mol/L。如果反应向逆反应方向进行,则c1只要大于0即可,所以选项C也不正确,答案选D。
,解得c1∶c2=1∶3,即二者的起始浓度之比恰好等于相应的化学计量数之比,所以X、Y的转化率相等,A不正确,D正确;反应速率之比是相应的化学计量数之比,所以平衡时,Y和Z的生成速率之比为3∶2,B不正确;如果反应向正反应方向进行,则(c1-0.1)×2=0.08-c3,解得c1<0.14 mol/L。如果反应向逆反应方向进行,则c1只要大于0即可,所以选项C也不正确,答案选D。
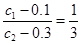 ,解得c1∶c2=1∶3,即二者的起始浓度之比恰好等于相应的化学计量数之比,所以X、Y的转化率相等,A不正确,D正确;反应速率之比是相应的化学计量数之比,所以平衡时,Y和Z的生成速率之比为3∶2,B不正确;如果反应向正反应方向进行,则(c1-0.1)×2=0.08-c3,解得c1<0.14 mol/L。如果反应向逆反应方向进行,则c1只要大于0即可,所以选项C也不正确,答案选D。
,解得c1∶c2=1∶3,即二者的起始浓度之比恰好等于相应的化学计量数之比,所以X、Y的转化率相等,A不正确,D正确;反应速率之比是相应的化学计量数之比,所以平衡时,Y和Z的生成速率之比为3∶2,B不正确;如果反应向正反应方向进行,则(c1-0.1)×2=0.08-c3,解得c1<0.14 mol/L。如果反应向逆反应方向进行,则c1只要大于0即可,所以选项C也不正确,答案选D。
练习册系列答案
相关题目
 C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题:
C(g)+D(g),在不同温度下,D的物质的量n(D)和时间t的关系如图。试回答下列问题: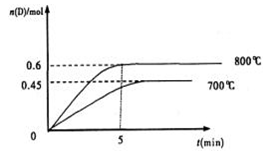
 2C(g) ΔH<0。
2C(g) ΔH<0。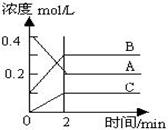
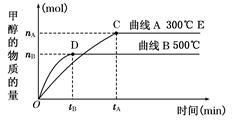
 C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为
C(g)+D(g),5 min后达平衡。已知该反应在此温度下平衡常数K=1,若温度不变的情况下将容器的体积扩大为原来的10倍,A的转化率不发生变化,则B的转化率为 N2O4(g);ΔH<0,在达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是 ( )
N2O4(g);ΔH<0,在达到平衡后,若分别单独改变下列条件,重新达到平衡后,能使平衡混合气体平均相对分子质量减小的是 ( ) CO2+H2.当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是
CO2+H2.当反应达到平衡时,CO的体积分数为x。若维持容器的体积和温度不变,起始物质按下列四种配比充入该容器中,达到平衡时CO的体积分数大于x的是 qD(g)的△H<0,m+n>q,在一个体积固定的密闭容器中反应达到平衡时,下列说法正确的是
qD(g)的△H<0,m+n>q,在一个体积固定的密闭容器中反应达到平衡时,下列说法正确的是