题目内容
下列叙述中不正确的是( )
| A、氯化钠的晶体结构为非等径圆球密堆积 |
| B、晶体尽量采取紧密堆积方式以使其变得比较稳定 |
| C、因为共价键有饱和性和方向性,所以原子晶体不遵循“紧密堆积”原则 |
| D、金属铜和镁均以ABAB方式密堆积 |
考点:不同晶体的结构微粒及微粒间作用力的区别
专题:化学键与晶体结构
分析:A.氯化钠中,Cl-的半径大于Na+,使得其晶体结构为非等径圆球的密堆积;
B.晶体倾向于能量最低,因此在以没有方向性和饱和性的作用力结合形成晶体时,会尽量采取紧密堆积方式,以使其变得比较稳定;
C.原子晶体是原子以具有方向性和饱和性的共价键结合形成的,不能紧密堆积,不遵循“紧密堆积”原理;
D.铜采取“…ABCABC…”型最密堆积,镁采取“…ABAB…”型最密堆积.
B.晶体倾向于能量最低,因此在以没有方向性和饱和性的作用力结合形成晶体时,会尽量采取紧密堆积方式,以使其变得比较稳定;
C.原子晶体是原子以具有方向性和饱和性的共价键结合形成的,不能紧密堆积,不遵循“紧密堆积”原理;
D.铜采取“…ABCABC…”型最密堆积,镁采取“…ABAB…”型最密堆积.
解答:
解:A.氯化钠中,Cl-的半径大于Na+,使得其晶体结构为非等径圆球的密堆积,相当于由半径大的Cl-最密堆积,然后Na+再填入Cl-形成的空隙中,故A正确;
B.在以没有方向性和饱和性的作用力结合形成晶体时,晶体尽量采取紧密堆积方式以使其变得比较稳定,故B正确;
C.因为共价键有饱和性和方向性,所以原子晶体不能紧密堆积,不遵循“紧密堆积”原理,故C正确;
D.铜采取“…ABCABC…”型最密堆积,镁采取“…ABAB…”型最密堆积,堆积方式不同,故D错误;
故选D.
B.在以没有方向性和饱和性的作用力结合形成晶体时,晶体尽量采取紧密堆积方式以使其变得比较稳定,故B正确;
C.因为共价键有饱和性和方向性,所以原子晶体不能紧密堆积,不遵循“紧密堆积”原理,故C正确;
D.铜采取“…ABCABC…”型最密堆积,镁采取“…ABAB…”型最密堆积,堆积方式不同,故D错误;
故选D.
点评:本题主要考查了晶体的堆积方式与原因,难度不大,注意对应知识的掌握.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、25℃时,pH=7的NH4Cl与NH3?H2O混合溶液:c(H+)=c(OH-)=c(NH4+)=c(Cl-) |
| B、0.1mol/L Na2S溶液:c(OH-)=c(H+)+c(HS-)+c(H2S) |
| C、25℃时,pH=2的HCOOH与pH=12的NaOH等体积混合:c(HCOO-)+c(H+)>c(Na+)+c(OH-) |
| D、0.1mol/L Na2CO3溶液与0.1mol/L NaHCO3溶液等体积混合:2c(CO32-)+2c(HCO3-)+2c(H2CO3)=3c(Na+) |
有一瓶无色气体,可能含有H2S、CO2、HCl、NO2、SO2中的若干种,将其通入氯水中,得无色透明液,将此溶液分成两份,向其中一份加入盐酸酸化的BaCl2溶液有白色沉淀;向另一份中加入HNO3酸化的AgNO3溶液有白色沉淀产生,则下列结论正确的是( )
| A、肯定有CO2和SO2 |
| B、可能有NO2、CO2 |
| C、肯定没有NO2、H2S、HCl |
| D、以上结论均不正确 |
能正确表示下列反应的离子方程式是( )
| A、石灰石溶于醋酸:CaCO3+2H+=Ca2++CO2↑+H2O |
| B、氯化铝溶液中加入过量的氨水:Al3++3NH3?H2O=Al(OH)3↓+3NH4+ |
| C、硫酸亚铁溶液中通入足量的氯气:Fe2++Cl2=Fe3++2Cl- |
| D、锌与稀硝酸反应:Zn+2H+=Zn2++H2↑ |
下列反应中,属于加成的是( )
A、C2H5OH
| |||
| B、CH3CH3+Cl2→CH3CH2Cl+HCl | |||
| C、CH3-CH=CH2+Br2→CH3-CHBr-CH2Br | |||
D、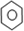 +H2S04 +H2S04
 +H2O +H2O |
下列操作正确的是( )
| A、用氨水清洗做过银镜反应的试管 |
| B、向放有电石的圆底烧瓶中,滴入饱和食盐水可产生乙炔气体 |
| C、将2%的NaOH溶液4至5滴,滴入2mL 10%的CuSO4溶液中制得Cu(OH)2悬浊液,加入乙醛溶液加热,用以检验醛基存在 |
| D、取一部分淀粉水解液,往其中加入适量的新制备的氢氧化铜悬浊液,加热一段时间后,未见砖红色沉淀产生,说明淀粉未水解 |
由德、法、美及波兰等多国科学家组成的科研小组合成了非常罕见的
Fe原子,下列说法不正确的是( )
45 26 |
A、可以用KSCN溶液检验
| ||||
B、
| ||||
C、
| ||||
D、
|
甲醛(H2C=O)在Ni催化作用下加氢可得甲醇(CH3OH),以下说法中不正确的是( )
| A、甲醇分子内C原子的杂化方式为sp3杂化 |
| B、甲醇分子内的O-C-H键角大于甲醛分子内的O-C-H键角 |
| C、甲醛分子内C原子上无孤对电子 |
| D、甲醛分子两个C-H键夹角小于120° |