题目内容
在室温下,向一定量的稀氨水中逐滴加入物质的量浓度相同的稀盐酸,直至盐酸过量。请回答下列问题。
(1)在实验过程中水的电离程度的变化趋势是先_______后________;(填“增大”、“减小”或“不变”)
(2)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH,请将表中空格部分填上相应的内容,将表格补充完整。
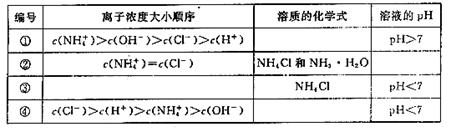
(1) 增大 减小 (2) ①NH3·H2O和NH4Cl ②pH=7 ③c(Cl-)>c(NH4+)>c(H+)>c(OH-) ④ HCl 和 NH4Cl
解析:
本题考查了电解质溶液中电解质的电离、水解和离子浓度问题。属于中等难度题。
![]()
![]() (1)由NH3·H2O NH4Cl HCl过量过程中,NH4+水解使水的电离程度增大,HCl过量使H+浓度增大抑制水的电离,使水的电离程度减小,所以水的电离是先增大后减小的。
(1)由NH3·H2O NH4Cl HCl过量过程中,NH4+水解使水的电离程度增大,HCl过量使H+浓度增大抑制水的电离,使水的电离程度减小,所以水的电离是先增大后减小的。
(2) ①中因c(NH4+)最大,所以溶质为NH3·H2O和NH4Cl;②中由电荷守恒可得溶液pH=7;③中由NH4Cl水解可得离子浓度关系;④中c(Cl-)最大,因此溶质为HCl 和 NH4Cl。

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
在室温下,向一定量的稀氨水中逐滴加入物质的量浓度相同的稀盐酸,直至盐酸过量。请回答下列问题。
(1)在实验过程中水的电离程度的变化趋势是先____________后____________(填“增大”“减小”或“不变”)。
(2)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序、对应溶质的化学式和溶液的pH,请将表中空格部分填上相应的内容,将表格补充完整。
编号 | 离子浓度大小顺序 | 溶质的化学式 | 溶液的pH |
① | c( |
| pH>7 |
② | c( | NH4Cl和NH3·H2O |
|
③ |
| NH4Cl | pH<7 |
④ | c(Cl-)>c(H+)>c( |
| pH<7 |
室温下,向一定量的稀氨水中逐滴加入物质的量浓度相同的盐酸,直至盐酸过量.
(1)在滴加过程中,水的电离程度的变化是先______后______(填“增大”、“减小”或“不变”);
(2)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和溶液的pH.
试填写表中空白:
(1)在滴加过程中,水的电离程度的变化是先______后______(填“增大”、“减小”或“不变”);
(2)在下表中,分别讨论了上述实验过程中离子浓度的大小顺序,对应溶质的化学式和溶液的pH.
试填写表中空白:
| 离子浓度的关系 | 溶质的化学式 | 溶液的pH | |
| ① | [NH4+]>[Cl-]>[OH-]>[H+] | ______ | pH>7 |
| ② | [NH4+]=[Cl-] | NH4Cl、NH3?H2O | ______ |
| ③ | ______ | NH4Cl | pH<7 |
| ④ | [Cl-]>[H+]>[NH4+>[OH-] | ______ | pH<7 |
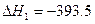 kJ·mol-1
kJ·mol-1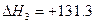 kJ·mol-1
kJ·mol-1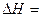 。
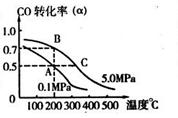
。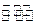 CH3OH(g);CO的转化率(
CH3OH(g);CO的转化率( )与温度、压强的关系如右图所示。
)与温度、压强的关系如右图所示。