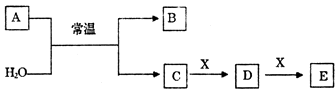
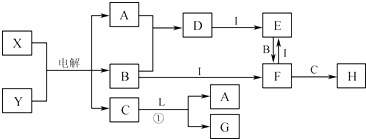
题目内容
【题目】确定有机物的组成及结构的方法很多.
(1)测定某有机物的相对分子质量,常用的方法是(填字母).a.质谱法 b.燃烧法 c.核磁共振氢谱法
(2)下列有机物中核磁共振氢谱只有1个峰的是(填字母).a.甲苯 b.新戊烷c.乙醚
(3)1mol下列物质完全燃烧时,消耗3mol O2的是(填字母).a.乙炔 b.丁烷 c.乙醇.
【答案】
(1)a
(2)b
(3)c
【解析】解:(1)质谱仪其实是把有机物打成很多小块,会有很多不同的分子量出现,其中最大的那个就是该有机物的分子量,故选a;(2)a.甲苯分子中有2种氢原子,核磁共振氢谱有2个峰,故a错误;b.新戊烷分子中有1种氢原子,核磁共振氢谱有1个峰,故b正确;c.乙醚分子中有2种氢原子,核磁共振氢谱有2个峰,故c错误;故选b;(3)设有机物的化学式为CxHyOz , 1mol该有机物消耗的氧气的物质的量为(x+ ![]() ﹣
﹣ ![]() )mol,则a.1mol乙炔消耗氧气为1mol×(2+
)mol,则a.1mol乙炔消耗氧气为1mol×(2+ ![]() )=2.5mol; b.1mol丁烷消耗氧气为1mol×(4+
)=2.5mol; b.1mol丁烷消耗氧气为1mol×(4+ ![]() )=6.5mol; c.1mol乙醇消耗氧气为1mol×(2+
)=6.5mol; c.1mol乙醇消耗氧气为1mol×(2+ ![]() ﹣
﹣ ![]() )=3mol;故选c.
)=3mol;故选c.

 名题训练系列答案
名题训练系列答案 期末集结号系列答案
期末集结号系列答案【题目】在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)CO(g)+H2O(g),其化学平衡常数K和温度t的关系如下表:
t℃ | 700 | 800 | 830 | 1000 | 1200 |
K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为;
(2)反应是反应.(选填“吸热”、放热).
(3)能判断该反应是否达到化学平衡状态的依据是 . a.容器中压强不变 b.混合气体中c(CO)不变
c.v正(H2)=v逆(H2O) d.c(CO2)=c(CO)
(4)某温度下,平衡浓度符合下式:c(CO2)c(CH2)=c(CO)c(H2O),试判断此时的温度为℃
【题目】某校课外活动小组为了探讨铜与硝酸的反应设计了如下实验。
(1)甲同学欲探究铜与稀硝酸反应产生的气体主要是NO,设计装置如图所示(加热装置和固定装置均已略去)。图中K为止水夹(处于关闭状态),F是含有一半空气的注射器。
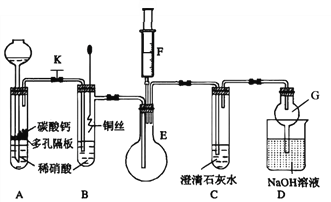
请回答有关问题:
①装置A中进行反应时打开止水夹K,当装置C中_________时,关闭止水夹K,试分析这样操作的目的是________,A中反应的离子方程式为______________。
②在完成①中的“操作”后,将装置B中铜丝插入稀硝酸,并微热之,观察到装置B中的现象是__________________,B中反应的离子方程式为____________________。
③为进一步证明产物是NO,将注射器F中的空气推入E中,看到的现象是_________________。
④装置G的作用是_____________________。
(2)同学们发现铜与稀、浓硝酸反应所得溶液的颜色不同,并记录如下:
将1 g细铜丝放入盛有10 mL的1 mol·L-1 HNO3溶液的试管中加热 | 铜丝表面有无色气体逸出,溶液变为天蓝色 |
将1 g细铜丝放入盛有10 mL的14 mol·L-1HNO3溶液的试管中 | 产生大量红棕色气体,溶液变为绿色,绿色由深到浅,未见到蓝色 |
有同学认为是铜与浓硝酸反应的溶液中溶解了生成的气体,也有同学认为是溶液中剩余硝酸浓度较大所致,同学们分别设计了以下4个实验来判断该看法是否正确,以下方案中可行的是(选填序号字母)____________。
a. 向上述绿色溶液中通入氮气,观察颜色变化
b. 加水稀释上述绿色溶液,观察颜色变化
c. 向饱和的硝酸铜溶液中不断滴加14 mol·L-1HNO3溶液
d. 向饱和硝酸铜溶液中通入浓硝酸与铜反应产生的气体,观察颜色变化