题目内容
【题目】关于离子化合物NH5(H有正价和负价)下列说法正确的是( )
A.N为+5价B.阴阳离子个数比是1:1
C.阴离子为8电子稳定结构D.阳离子的电子数为11
【答案】B
【解析】
根据题干信息知,氢有正价和负价,所以NH5可以写成NH4H,其中铵根离子中氮元素化合价为-3价,氢元素化合价为+1价,后面有-1价氢离子。
A.氮元素的化合价为-3价,故A错误;
B.阴阳离子个数比为1:1,故B正确;
C.阴离子是H-,为2电子稳定结构,故C错误;
D.阳离子为铵根离子,电子数为10,故D错误;
答案选B。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案【题目】S2Cl2和SCl2均为重要的化工原料。
已知:I.S2(l) + Cl2(g)![]() S2Cl2(g) ΔH1;
S2Cl2(g) ΔH1;
II. S2Cl2 (g) +Cl2 (g)![]() 2SCl2 (g) ΔH2;
2SCl2 (g) ΔH2;
III.相关化学键的键能如下表所示:
化学键 | S—S | S—Cl | Cl—Cl |
键能/kJ mol-1 | a | b | c |
请回答下列问题:
(1) SCl2的结构式为______________________。
(2)若反应II正反应的活化能E=dkJ·mol-1,则逆反应的活化能E2=_______kJ·mol-1(用含a、b、c、d的代数式表示)。
(3)—定压强下,向10 L密闭容器中充入1molS2Cl2和1mol Cl2,发生反应II。Cl2与SCl2的消耗速率(v)与温度(T)的关系如图所示:
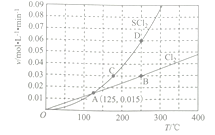
①A、B、C、D四点对应状态下,达到平衡状态的有 ____________(填字母),理由为__________。
②ΔH2_______________0(填“>” “<” 或“=”)。
(4)已知:ΔH1<0。向恒容绝热的容器中加入一定量的S2(l)和Cl2(g),发生反应I,5 min时达到平衡。则3 min时容器内气体压强__________(填“>” “<” 或“=”)5 min时的压强。
(5)—定温度下,在恒容密闭容器中发生反应I和反应II,达到平衡后缩小容器容积,重新达到平衡后,Cl2的平衡转化率_________(填“增大”“减小”或“不变”),理由为_________________。